КОНСТРУИРОВАНИЕ ПРОДУЦЕНТОВ С ПОМОЩЬЮ ГЕННОЙ ИНЖЕНЕРИИ. ГЕНЕТИЧЕСКАЯ ИНЖЕНЕРИЯ РАСТЕНИЙ.
1. Сущность и задачи генной инженерии.
Для того, чтобы искусственным путем наделить какой-либо организм новыми наследственными свойствами, нужно ввести в него хотя бы один чужеродный ген, причем, необходимо приготовить (сконструировать) фрагмент чужеродной ДНК, содержащий этот нужный ген.
Генная инженерия, или техника рекомбинантных ДНК, — это совокупность приемов, позволяющих in vitro перенести генетический материал из одного организма(источника генов) в другой (реципиент) так, чтобы обеспечить наследование этих генов в новом для них организме.
Одной из главных задач генной инженерии является получение организмов с желаемыми свойствами. Одним из последних сверх достижений генной инженерии является создание искусственной клетки, о чем доложил 2010 году Крейг Вентер.
Методами генной инженерии возможно преодолевать межвидовые барьеры, то есть переносить гены и передавать отдельные наследственные признаки одних организмов другим (напр., от человека или животного — бактериям, растениям и др.). Получают генетически модифицированные микроорганизмы (трансгенные или рекомбинантные) обладающие сверхпродукцией для производства инсулина, соматотропина, интерферона и многих других белков.
2. Этапы получения генетически модифицированных микроорганизмов–продуцентов:
Iвыделение нужного (целевого) гена;
II встраивание гена в генетический элемент, способный к репликации (вектор);
III введение вектора в организм-реципиент;
VI идентификация (скрининг) и отбор клеток, которые приобрели желаемый ген или гены.
I Выделение нужного (целевого) гена. Выделение генов – один из главных этапов в генетической инженерии. Существует два основных способа получения гена: синтез и выделение из ДНК.
Синтез гена осуществляется 2-мя путями
А. Химико-ферментативный синтез генов (применяется наиболее часто).
Химическим путем синтезируют олигонуклеотиды или праймеры (короткие одноцепочечные фрагменты ДНК — 8-16 нуклеотидов), а гены синтезируют ферментативным методом с помощью ПЦР. Химический синтез генов возможен когда известен нуклеотидный состав (первичная структура) гена или первичная структура кодируемого геном полипептида.
Б. Синтез генов с помощью обратной транскрипциинамРНК. Выделяют мРНК соответствующего гена из полирибосом и используют ее в качестве матрицы для фермента ревертазы. Метод основан на универсальной способности обратных транскриптаз синтезировать двунитевую ДНК на однонитевых РНК-матрицах.
Гены также могут быть получены из уже созданных геномных библиотек, которые представляют собой совокупность фрагментов геномной ДНК какого-либо организма или из библиотек кДНК.
2)Выделение гена из ДНКклетки с нужными свойствами.Необходимо точно знать расположение гена и вырезать его при помощи рестриктаз. Каждая из рестриктаз узнает свой сайт рестрикции и разрезает ДНК либо внутри сайта, либо в непосредственной близости от него.Рестриктазы (своеобразные молекулярные ножницы), действуя на двухцепочечную ДНК, «узнают» в ней определенную последовательность нуклеотидов. Причем, каждая рестриктаза узнает только свою последовательность ДНК, прикрепляется к ней и разрезает ее в месте прикрепления. Рестриктазам безразлично, какую ДНК разрезать – человека или растения, бактерии или вируса, лишь бы в ней были распознаваемые участки.
Это значит, что две совершенно несхожих между собой последовательности ДНК (допустим из клеток слона и лягушки) при обработке одной и той же рестриктазой легко можно сшить (слепить) друг с другом.
II Встраивание гена в генетический элемент, способный к репликации (вектор).
Выделенный или синтезированный ген не может самостоятельно встраиваться в ДНК клетки-мишени и тем более начинать функционировать. Для переноса целевого гена создают специальную конструкцию — вектор, несущий полученный ген и способный встраиваться в геном клетки. Генетический вектор – это молекула ДНК или РНК, которые способны переносить в клетку чужеродную ДНК, обеспечить еѐ амплификацию и интеграцию в геном.
1.Требования к генетическим векторам:
— вектор должен быть небольшим и содержать сайты рестрикции для нескольких рестриктаз, должен обладать определенной емкостью;
— вектор должен иметь точку начала репликации (ori), т.е. автономно реплицироваться, накапливаться в многочисленных копиях в клетке хозяина и сохраняться в дочерних клетках при делении материнской;
— иметь функциональный генпромотор (прокариотический или эукариотический), способный экспрессироваться в клетке;
— должен иметь маркерный ген, позволяющий различать гибридные клетки для эффективной селекции;
— должен быть способным передаваться в клетку соответствующего организма.
2. Характеристика векторов для переноса генетической информации в прокариотические клетки.
В качестве прокариотических векторов чаще используют плазмидыбактерий, бактериофаги.
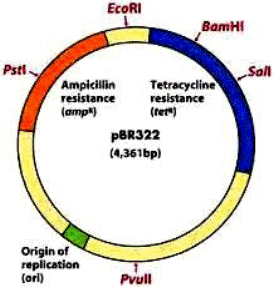
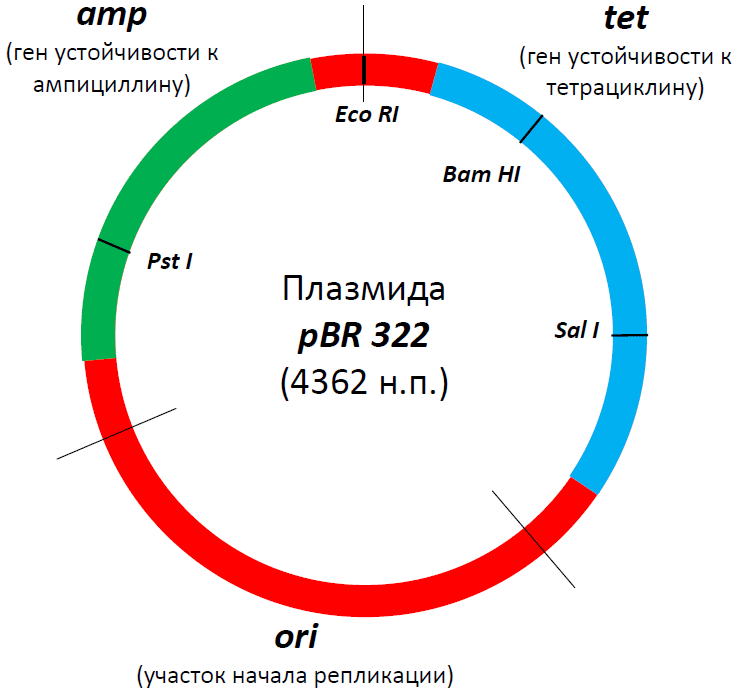
Плазмидыбактерий способны реплицироваться независимо от хромосомы это их главное свойство.Плазмиды могут быть выделены из клетки и использованы в неповрежденном, нативном состоянии. В векторной плазмиде E.colipBR322есть маркерные гены устойчивости к ампициллину и к тетрациклину. Бактериальные клетки, содержащие такой вектор, устойчивы одновременно к ампициллину и тетрациклину. Плазмидные векторы удобны для клонирования небольших фрагментов (до 10 тыс. пар оснований) геномов, т.е. плазмидные векторы обладают небольшой емкостью.
Бактериофаги – вирусы бактерийспособны встраиваться в геном клетки хозяина (вызывать лизогенизацию).
Бактериофаги широко распространены в природе — их выделяют из воды, почвы, организмов различных животных и человека. Большинство фагов ДНК-содержащие вирусы, имеют смешанный тип симметрии капсида. Широко используют векторы на основе бактериофагов E.coli —λ и М13. Из ДНК фага удаляют области, не существенные для репликации в клетках E.coli, и оставляют сайты, предназначенные для встраивания фага в геном клетки хозяина (фаговый вектор должен проникнуть в клетку и встроиться в геном). В эту же область встраивают целевой и маркерные гены. На основе бактериофага λ можно сконструировать векторы емкостью до 25 т.п.н.
3. Характеристика векторов для переноса генетической информации в эукариотические клетки.
В качестве эукариотических векторов используют вирусы животных и растений,Tiплазмиды агробактерий (Agrobakterium tumefaciens), а также искусственно сконструированные векторы, способные реплицироваться как в бактериальных, так и в эукариотических клетках (челночные векторы).
Длина плазмиды 4361 п.н., она имеет 2 гена устойчиво-сти к антибиотикам: ампициллину (Ampr), тетрациклину (Tetr), а также сайты для рестриктаз: — BamHI (Bacillus amyloliquefaciens H) — HindIII (Haemophilus influenzae d) — SalImonella (Streptomyces albus) — PstI (Providencia stuartii) — EcoRI (E.Coli) (Escherichia coli).
4.Создание генетической конструкции.
Очищенную кольцевую плазмиду E.coli pBR322 обрабатывают ферментом рестриктазой BamH1, которая специфически разрезает плазмиду в единственном сайте, расположенном в гене устойчивости к тетрациклину, так что образуется линейная молекула с липкими концами. Такие молекулы смешивают с подготовленным участком ДНК (с нужным геном), содержащим комплементарные липкие концы.
Поскольку липкие концы этих двух ДНК взаимно комплементарны, они спариваются с образованием гибридных молекул. Далее смесь обрабатывают ДНК-лигазой для сшивания комплементарных концов нужного гена и вектора.
При включении фрагментов ДНК в участок гена резистентности к тетрациклину, устойчивость к тетрациклину из-за этой вставки нарушается, и все рекомбинантные плазмидысохраняют устойчивость только к ампициллину. Таким образом, высевая клетки на среды с антибиотиками, можно отобрать клоны, содержащие рекомбинантные молекулы ДНК.
Гибридные векторы, содержащие ДНК фага и плазмиды- космиды и фазмиды.
Космиды – плазмидные векторы, в которые встроен участок генома фага λ, обеспечивающий возможность упаковки этой молекулы ДНК в фаговую частицу. Фаговые частицы обеспечивают хорошее проникновение гибридной ДНК в клетку (путем инъекции), после чего происходит замыкание ДНК в кольцо по липким концам и репликация ее по плазмидному типу.
Фазмиды также являются гибридами между фагом и плазмидой. После встройки чужеродной ДНК могут в одних условиях развиваться как фаги, в других – как плазмиды.
Векторы на основе РНК-содержащих вирусов или ретровирусов (Retroviridae). Они легко интегрируют в геном клетки-хозяина, тем самым обеспечивая долговременную экспрессию необходимого гена. Попадая внутрь клетки, ретровирусная РНК превращается в ДНК путем хорошо теперь известного процесса обратной транскрипции. Эта ДНК встраивается в геномную ДНК и с этого момента становится неотъемлемой частью генома клетки (является провирусом). Инфицирование организма ретровирусами – это своего рода естественно-природный механизм генетической модификации клетки. Наиболее часто в качестве вектора применяют вирус лейкемии мышей.
Векторы на основе ДНК-геномных вирусов. Векторы, созданные на основе ДНК-вирусов обладают большими размерами по сравнению с РНК-геномными вирусами и поэтому могут вмещать фрагменты ДНК (трансгены) длиной до 35 000 пар оснований. С точки зрения переноса чужеродного ДНК в организм реципиента удобными оказались так называемые «челночные векторы», способные реплицироваться как в клетках животных, так и в клетках бактерий. Их получают, сшивая друг с другом большие сегменты вирусов животных и бактерий (например, SV40 и pBR322) так, чтобы области, ответственные за репликацию ДНК, остались незатронутыми. Это позволяет проводить основные операции по конструированию вектора в бактериальной клетке, а затем полученную рекомбинантную ДНК использовать для клонирования генов в животной клетке.
- Молекулярное клонирование, или как засунуть в клетку чужеродный генетический материал
- Молекулярное клонирование, или как засунуть в клетку чужеродный генетический материал
- «Био/мол/текст»-2011
- Вставка
- Вектор
- Плазмида
- Размножение
- Разрезание
- Селекция
- Промоторы
- Трансляция белка
- Плазмидные базы данных
- Другие векторы
- Вставляем ген в плазмиду
- Выделяем вектор
- Как засунуть вектор в клетки
- Вещества-проводники
- Дырки в мембране
- Овечки в волчьей шкуре
- Ретро
- Ленти
- Адено
- Последний шаг
- Генная инженерия для биотехнологических производств
Молекулярное клонирование, или как засунуть в клетку чужеродный генетический материал
30 октября 2011
Молекулярное клонирование, или как засунуть в клетку чужеродный генетический материал
- 28031
- 14,4
- 13
- 23
Клонирование овечек имеет лишь самое опосредованное отношение к молекулярному клонированию. На фоне овечки Долли показана плазмида phMYT1L-N106.
коллаж автора статьи
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Огромное количество биологических исследований начинается с того, что в клетку вносится чужеродный генетический материал. Это действие называется молекулярным клонированием. С его помощью можно получить генетически модифицированные организмы, включить и выключить отдельные гены или определить роль конкретного белка в каком-нибудь процессе. Можно сказать, что молекулярное клонирование — это краеугольный камень, основа основ, фундамент, без которого множество замечательных методик было бы неосуществимо. Однако засунуть в клетку «неродную» ДНК не так-то просто: это длинный, трудоемкий и многоэтапный процесс. Молекулярному клонированию посвящены толстые книги, но, тем не менее, я попробую хотя бы немного рассказать о том, что это такое, и что нужно для того, чтобы все получилось.
«Био/мол/текст»-2011
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2011 в номинации «Лучшая обзорная статья».
Вставка
Раз мы собираемся вставлять в клетки какой-то ген, то самый первый, очевидный шаг, который нам нужно сделать, — этот ген как-нибудь получить, причем желательно в больших количествах (поскольку все методики несовершенны, бóльшая часть копий этого гена бесследно пропадет по дороге нецелевым способом). Чужеродный ген, вносимый в клетку, называется «геном-вставкой» или просто «вставкой». Получить его можно несколькими способами.
Во-первых, мы можем просто выделить его из того генома, к которому он принадлежит. Допустим для простоты, что наша вставка — это какой-нибудь ген слона. Тогда нам нужно:
- получить образец тканей слона;
- извлечь из этого образца ДНК;
- вычленить из этой ДНК интересующий нас ген и получить его в больших количествах (для этого используется ПЦР ). [Заметим в скобках, что получение гена с помощью ПЦР возможно, только если мы знаем его нуклеотидную последовательность или хотя бы последовательность его начала и окончания (для того, чтобы можно было синтезировать праймеры). Если же все это нам неизвестно, то придется сначала анализировать слоновий геном.]
Подробнее с методом ПЦР и другими основными молекулярно-биологическими методиками можно ознакомиться в статье «Важнейшие методы молекулярной биологии и генной инженерии»; с геномными исследованиями — в статье «Геном человека: как это было и как это будет». — Ред.
Во-вторых, вполне возможно, что нужный нам ген уже был выделен из генома слона и присутствует в библиотеке генов. Тогда нашу вставку можно будет получить оттуда (с этим, на самом деле, тоже придется повозиться, но меньше, чем в первом случае).
И наконец, в-третьих, не обязательно использовать в качестве вставки уже существующий ген. Если исследователь собирается работать с каким-нибудь геном, который является плодом его фантазии и не встречается в природе, то он может синтезировать его искусственно.
Вектор
Запускание в клетку «одинокой» вставки (то есть, гена самого по себе, безо всякого сопровождения) — дело совершенно бесперспективное. В клетке плавает множество расщепляющих ДНК ферментов (нуклеаз), которые с радостью набросятся на беззащитную вставку и разрежут ее на кусочки, в результате чего она бесславно исчезнет, не успев совершить ничего полезного, а клонирование провалится.
Поэтому, чтобы защитить вставку, ее встраивают в специальное «транспортное средство», которое называется вектором. В самом элементарном случае вектор — это просто последовательность ДНК, в которую вшивается наша вставка, и которая помогает ей не пропасть в клетке и выполнить свое предназначение. Существует несколько видов векторов, но среди исследователей самой большой (и заслуженной) любовью пользуется один из них — плазмиды. С них-то мы и начнем.
Плазмида
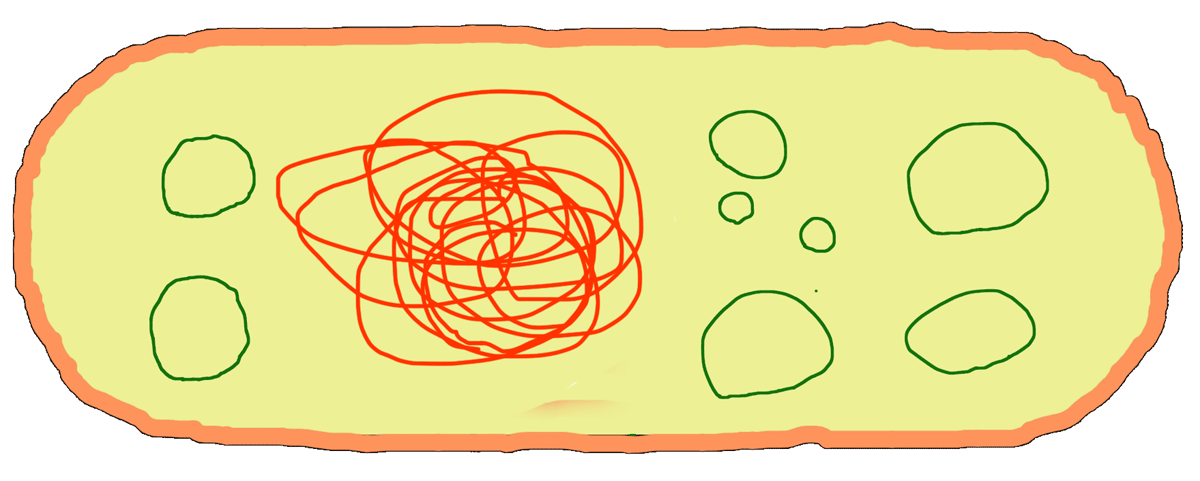
Плазмида — это довольно короткая и обычно кольцевая молекула ДНК, которая плавает в цитоплазме бактериальной клетки (зеленые кружочки на рис. 1). Плазмиды не связаны с бактериальной хромосомой, они могут реплицироваться независимо от нее, могут «выплевываться» бактерией в окружающую среду или, наоборот, из этой окружающей среды «проглатываться». С помощью плазмид бактерии обмениваются друг с другом генетической информацией, — например, передают соседям устойчивость к какому-нибудь антибиотику.
Рисунок 1. В бактериальной клетке наряду с бактериальной хромосомой плавает еще и множество плазмид.
рисунок автора статьи
Плазмиды существуют внутри бактерий в естественных условиях, поэтому никто не может помешать исследователю искусственно синтезировать плазмиду, которая будет обладать нужными для него свойствами, вшить в нее вставку (или несколько) и запустить в клетку. Плазмида — это, можно сказать, «болванка» для молекулярного биолога. Поэтому плазмиды стараются сделать как можно более универсальными и подходящими для всех случаев жизни.
Для того, чтобы из плазмиды получился рабочий вектор, она должна обладать некоторыми важными характеристиками.
Размножение
Прежде всего, плазмида обязательно должна в клетке размножаться, реплицироваться, потому что иначе она быстро подвергнется деградации, а вместе с ней исчезнет и ген-вставка. Для этого в ней должна быть специальная последовательность под названием «точка начала репликации», с которой и начинается удвоение ДНК. У разных видов живых существ эти точки имеют разную нуклеотидную последовательность. Поэтому, если мы хотим создать плазмиду, которая бы реплицировалась сразу в двух видах клеток (например, и в дрожжевых, и в бактериальных), то нам надо вставить в нее две точки начала репликации.
Разрезание
Кроме того, в ДНК плазмиды должны быть участки, в которых ее можно будет разрезать, чтобы вшить туда вставку. В качестве «ножниц» используются особые ферменты — рестриктазы. Они прекрасны тем, что режут ДНК не где попало, а в строго определенных местах, которые называются сайтами рестрикции (каждая рестриктаза распознает только свой сайт и только в нем (или возле него) разрезает ДНК). Обычно в плазмиду ставят множество разных сайтов рестрикции, расположенных в разных точках, — благодаря этому ее можно будет разрезать в нужном месте нужной рестриктазой. Участок ДНК, на котором собрано несколько сайтов рестрикции, называется полилинкером.
Селекция
Процесс, при котором бактерия «глотает» плазмиду, именуется трансформацией. В естественных условиях трансформироваться может в каждый момент времени не вся популяция бактерий, а только ее часть — компетентные клетки. Существуют лабораторные методы, с помощью которых можно искусственно увеличить количество компетентных клеток (некоторые из них описаны ниже в главе «Как засунуть вектор в клетки»), однако, все равно, стопроцентная компетентность для бактериальной культуры — вещь недостижимая.
Так что, добавляя плазмиду к бактериям, мы заранее должны смириться с тем, что бóльшая часть бактериальных клеток так и останется бесплазмидной, нетрансформированной. Поэтому нам придется отделять зерна от плевел, — то есть, трансформированные клетки от всех остальных. Для этого используется простой, но остроумный прием.
Допустим, мы встроили в нашу плазмиду ген устойчивости к какому-нибудь антибиотику (такой ген называется селективным маркером). Теперь клетки, которые «съели» плазмиду, будут неуязвимы для этого антибиотика и смогут спокойно жить в его присутствии. В результате, чтобы выделить из всех бактерий, к которым мы добавили плазмиду, те, которые смогли эту плазмиду использовать по назначению, нам достаточно будет добавить к бактериальной культуре соответствующий антибиотик. Те клетки, которые нам нужны, смогут существовать и делиться в присутствии этого антибиотика, а остальные этого делать не смогут.
Существуют и другие способы провести селекцию. Можно, например, поместить сайт рестрикции не внутрь гена антибиотика, а внутрь какого-нибудь «заметного» гена (скажем, такого, в присутствии которого бактериальные культуры меняют цвет). В результате можно будет отличить нужные колонии от ненужных просто на глаз, безо всяких манипуляций. По такому принципу работает, например, очень модная сейчас система бело-голубой селекции.
Если мы собираемся работать только на бактериях, то всем вышесказанным дело и ограничится. Однако если конечная наша цель — засунуть вектор в эукариотические клетки (например, клетки млекопитающих), то нам предстоит еще один этап селекции.
Дело в том, что в большинстве эукариотических клеток плазмиды живут недолго и быстро подвергаются деградации. Поэтому, даже если мы заставили клетку «съесть» плазмиду, не стоит питать надежды, что наша вставка теперь останется в этой клетке навсегда. Скорее всего, она успеет только немного поэкспрессироваться, прежде чем содержащий ее вектор будет пойман нуклеазой и разрезан на кусочки. Однако если вектор случайно смог встроиться в геном (это событие очень редкое, но не невероятное), то наша вставка, можно сказать, пустит в этой клетке корни — причем не только в ней самой, но и во всех ее потомках. И для того, чтобы выделить из всех клеток те, которые имеют вектор в своем геноме, нам понадобится еще один селективный маркер — ген устойчивости к какому-нибудь эукариотическому антибиотику (потому что бактериальные антибиотики, как правило, на клетки эукариот не действуют). Добавив соответствующий антибиотик (например, генетицин) к среде, в которой культивируются клетки, мы через некоторое время получим популяцию только тех клеток, в геноме которых сидит наш вектор.
Промоторы
Перед каждым рабочим геном находится короткий участок ДНК под названием промотор. Именно сюда прикрепляется фермент РНК-полимераза, который синтезирует РНК на матрице ДНК, что является первым и абсолютно необходимым этапом в экспрессии гена. Если у гена нет промотора, его экспрессию запустить невозможно, и он так и останется «молчащим». Можно сказать, что ген без промотора — это все равно, что машина без педали газа. Поэтому в нашей плазмиде обязательно должен быть хотя бы один промоторный участок, под контроль которого можно будет поставить ген-вставку.
А промоторы бывают разные.
Во-первых, они различаются по своей силе. Некоторые вызывают бурную транскрипцию подконтрольного гена, другие — совсем вялую.
Во-вторых, у прокариот и эукариот промоторы отличаются. Прокариотические промоторы не работают в эукариотических клетках и наоборот. Поэтому будет Ужасной Ошибкой поставить тот ген, который должен, экспрессироваться в бактериальных клетках, под эукариотический промотор — это все равно, что оставить его без промотора вообще.
В-третьих, у эукариот есть несколько типов РНК-полимеразы — они обеспечивают синтез различных видов РНК. И каждый тип РНК-полимеразы распознает только свои промоторы и «не видит» чужие. Поэтому, в зависимости от того, какую именно РНК кодирует наша вставка (например, матричную или, наоборот, шпилечную, а может, и вовсе рибосомальную), нам нужно подбирать и тип промотора, который мы будем ставить в плазмиду.
И, наконец, в-четвертых, разные промоторы включаются по-разному. Некоторые активны постоянно. Другие активизируются только при определенных условиях — например, при повышении окружающей температуры или появлении в клетке каких-то веществ. К тому же, у многоклеточных организмов в каждой ткани включены одни промоторы и выключены другие. Можно, например, подобрать такой промотор, который будет активен только в нейронах. Или только в нейронах головного мозга. Или только в нейронах головного мозга, относящихся к одному из подкорковых ядер. Или только в крохотной субпопуляции нейронов головного мозга, относящейся к одному из подкорковых ядер. И сужать этот круг можно почти до бесконечности.
Знание всего этого дает исследователю удивительную свободу. Подобрав в плазмиду подходящий промотор, он сможет творить с экспрессией гена-вставки почти все, что ему заблагорассудится. Ну, скажем, сделать так, чтобы он экспрессировался сильно, только в мышечных клетках и только в ответ на повышение температуры.
Трансляция белка
Засовывая вектор в клетку, ученый может хотеть двух разных вещей:
- чтобы происходила только транскрипция гена-вставки (то есть, синтез РНК на матрице ДНК — например, этого достаточно, если в клетку вносится какая-нибудь некодирующая РНК);
- чтобы происходила и транскрипция, и трансляция гена-вставки (то есть, экспрессия кодируемого вставкой белка).
В первом случае вектор называется транскрипционным, во втором — экспрессионным. Экспрессионные векторы обычно немного сложнее транскрипционных, потому что в них присутствуют:
- Консенсусная последовательность Козак. Это длинное имя носит короткий (примерно в 10 нуклеотидов) фрагмент в самом начале молекулы матричной РНК, который через белки-посредники обеспечивает связывание этой мРНК с рибосомой (без чего, как нетрудно догадаться, синтез белка невозможен). Последовательность Козак характерна только для эукариот, причем у представителей разных видов она немного отличается. Поэтому, создавая экспрессионный вектор, надо вставлять в него последовательность, которая характерна именно для того живого существа, в клетки которого мы собираемся вставлять вектор. Кроме того, последовательность Козак бывает сильной и слабой — то есть, приводящей к синтезу большого или малого количества белка. У прокариот роль последовательности Козак выполняет последовательность Шайна-Дальгарно, которая непосредственно (в смысле — без посредников, в отличие от последовательности Козак) соединяется с рибосомой, после чего и начинается синтез белка;
- Последовательность Козак находится перед вставляемым геном. А после него должны находиться еще несколько коротких участков, к которым присоединяются белки, выполняющие полиаденилирование — пришивание к концу свежесинтезированной РНК полиаденинового хвоста. Этот хвост выполняет несколько функций, в том числе, обеспечивает экспорт РНК в цитоплазму и помогает организации трансляции — то есть, если мы хотим обеспечить синтез белка на основе нашей РНК, нам без него не обойтись;
- мРНК, которая служит матрицей для синтеза белка, может быть транскрибирована только и исключительно РНК-полимеразой II типа. Поэтому нам нужно вставить в плазмиду именно тот промотор, который работает с этой РНК-полимеразой.
Итак, мы подобрали все необходимые для плазмиды кусочки. Но мало просто соединить их вместе — огромную роль играет их взаимное расположение. Например, сайты рестрикции должны быть не только многочисленны и разнообразны, но и находиться в «правильных» местах. При этом надо стараться, чтобы итоговая плазмида была как можно компактней, поскольку, во-первых, так она будет стабильнее, а во-вторых, охотнее «проглотится» клеткой. Одним словом, вы уже, наверное, поняли, что дизайн хорошей плазмиды — это тонкое и филигранное искусство (рис. 2).
Рисунок 2. Структура знаменитой плазмиды PBR322. В свое время это была, пожалуй, самая популярная плазмида во всем научном мире, а потом она стала основой для множества плазмид нового поколения. В ней есть участок начала репликации (ori), благодаря которому она может размножаться в клетках бактерии E. coli, гены устойчивости к двум антибиотикам — ампициллину (amp) и тетрациклину (tet), а также множество сайтов рестрикции (на самом деле их больше сорока, но здесь представлены только четыре — EcoRI, SalI, PstI, BamHI). Промоторные участки, к сожалению, не показаны, но они, разумеется, тут тоже есть. Некоторые сайты рестрикции находятся в генах устойчивости к ампициллину или тетрациклину, в результате чего и тот и другой сайт можно использовать в качестве второго селективного маркера. Например, если мы разрежем ген устойчивости к ампициллину с помощью рестриктазы PstI и вошьем в это место вставку, то тетрациклин будет первым селективным маркером, ампициллин — вторым, а селекция будет выглядеть так:
- Трансформируем бактерии, выращиваем их на среде с тетрациклином и выбираем только хорошо растущие клоны.
- Переносим эти клоны на среду с ампициллином и выбираем те, рост которых угнетается.
Если же мы вошьем вставку внутрь гена устойчивости к тетрациклину (разрезав его с помощью рестриктаз BamHI или SalI), то нам надо будет, наоборот, сначала посадить их на среду с ампициллином, а потом — с тетрациклином.
Плазмидные базы данных
За те несколько десятилетий, что существует методика молекулярного клонирования, были синтезированы тысячи разнообразных плазмид, из которых созданы базы данных (например, AddGene). В этих базах есть плазмиды на все случаи жизни — с разными типами точек начала репликации, разными полилинкерами, разными селективными маркерами и промоторами и так далее. Есть те, в которые можно вшить не одну вставку, а несколько, а есть даже такие, которые уже несут в себе некоторые особенно популярные вставки. Поэтому, как правило, исследователи не синтезируют плазмиду для клонирования самостоятельно, а покупают уже готовую. При необходимости купленную плазмиду можно «довести до ума», вставив или убрав определенные участки (а потом эту модифицированную плазмиду тоже добавить в базу данных). Иными словами, часто задача ученого сводится просто к тому, чтобы подобрать подходящую плазмиду.
Другие векторы
Плазмида — прекрасный вектор для относительно небольших вставок. Если ген-вставка слишком велик, то плазмида утрачивает стабильность, потому что ее участки начинают «перетасовываться» друг с другом и теряться при репликации, из-за чего она постепенно укорачивается. Поэтому в качестве вектора для длинных вставок используются более устойчивые конструкции. Например:
- Космида — гибрид плазмиды и фага (вируса, который заражает бактерии). По сути дела, это просто плазмида, в которую добавлены сайты для связывания с белками оболочки фага (они называются cos-сайтами, и именно благодаря им космиды получили свое название). Белковая оболочка делает космиду стабильнее, благодаря чему в нее можно загружать более длинные вставки;
- Искусственные хромосомы (человеческие, бактериальные, дрожжевые) — это сложные и крупные конструкции, являющиеся по сути микрохромосомами. Они относительно стабильны и при этом обладают гигантской емкостью: в них можно вставлять сразу несколько генов. Однако из-за огромных размеров их гораздо труднее засунуть в клетку;
- И, наконец, есть еще один вид векторов — вирусные. Этот вид настолько важен, что ниже ему будет посвящен целый раздел.
Вставляем ген в плазмиду
Допустим, исследователь подобрал подходящую плазмиду и получил нужную вставку. Теперь нужно соединить одно с другим, чтобы затем засунуть в клетки. Для этого достаточно совершить несколько простых действий.
Как уже говорилось, в плазмиде существует несколько сайтов рестрикции — то есть, участков, в которых ее может разрезать нужная рестриктаза. Нам нужно выбрать подходящий сайт, который будет находиться в том месте, куда мы собираемся вшивать вставку, а затем обработать плазмиду соответствующей рестриктазой.
После этого той же рестриктазой нужно обработать вставку, поскольку рестриктазы обычно оставляют выступающие концы на одной из нитей ДНК, и эти концы должны быть совместимы у вставки и плазмиды, чтобы они согласились соединиться. Если на кончиках вставки нет нужных сайтов рестрикции, то можно приделать к нему короткие ДНК-фрагменты с нужными сайтами рестрикции на концах.
И наконец, нам нужно соединить в одной пробирке плазмиду и вставку (предварительно очищенные от рестриктаз) и добавить к ним ДНК-лигазу, которая умеет лигировать (то есть, сшивать воедино) две молекулы ДНК. Конечно, в результате мы получим не только желанный вектор, в котором плазмида соединена со вставкой (назовем его чеширским котом с улыбкой), но и целый коктейль побочных продуктов — пустую плазмиду (кота без улыбки), замкнутую вставку (улыбку без кота), несколько сшитых между собой вставок (много улыбок) и так далее. В ходе селекции эти ненужные продукты отсеются, и у нас в руках останется только вектор.
Выделяем вектор
Итак, вначале мы проводим селекцию.
- Увеличиваем компетентность бактерий, добавляем к ним «коктейль», полученный в результате лигирования, а потом высеваем эти бактерии на среду с антибиотиком, который является нашим первым селективным маркером;
- Выбираем те бактериальные клоны, которые растут на среде с антибиотиком — они смогли съесть плазмиду со вставкой или хотя бы просто плазмиду (кота — с улыбкой или без);
- Проводим с этими клонами второй этап селекции, в зависимости от того, какой ген мы использовали в качестве второго селективного маркера. Например, если этот ген — устойчивость к другому антибиотику, то мы переносим бактерии на среду с этим антибиотиком и выбираем те клоны, рост которых угнетается, — они ухитрились проглотить не просто плазмиду, а плазмиду, в которую была вшита вставка (кота с улыбкой);
- Выращиваем полученную культуру бактерий.
И вот мы получили ее — бактериальную культуру, в которой живет созданный нами вектор. Вполне возможно, что это и было нашей конечной целью, и теперь мы, спокойные и счастливые, можем, например, включить в бактериях экспрессию гена-вставки и пожинать урожай синтезированных в результате белков.
Но если нам нужен чистый вектор, который можно будет потом засовывать в другие клетки, то у нас появляется проблема, которая кажется неразрешимой. Как вызволить вектор из бактерий? Ведь даже если мы выделим из этих бактерий ДНК, то помимо вектора получим еще и совершенно ненужную нам бактериальную хромосому.
Тут можно воспользоваться тем, что плазмидная ДНК имеет важные отличия от хромосомной: она, во-первых, гораздо меньше по размеру, а во-вторых, гораздо больше суперскручена. Поэтому можно подобрать такие условия, в которых бактериальные хромосомы будут осаждаться, в то время как плазмиды останутся плавать в растворе. Достаточно будет отцентрифугировать получившийся осадок (чтобы вся бактериальная ДНК прочно «упала на дно»), а затем уже из надосадочной жидкости выделить нашу плазмиду (обычно для этого используются специальные колонки, которые очень облегчают и ускоряют работу).
Как засунуть вектор в клетки
И вот наступил желанный миг. Исследователь держит в руке пробирку, в которой плещется прозрачная жидкость — столькими трудами полученный вектор. И тут перед ним встает преграда. Клетки, в которые он собирается засунуть свой вектор, отказываются его глотать.
Дело в том, что липидная мембрана, которой окружены клетки, обладает избирательной проницаемостью — то есть, она пропускает через себя одни частицы и не пропускает другие. Крупные заряженные молекулы (а именно таковой и является ДНК) через эту мембрану самопроизвольно пройти не могут. И если бактерии, например, умеют проглатывать плазмиды из внешней среды (как уже было сказано выше), то, скажем, клетки животных к этому совершенно не склонны. Поэтому для того, чтобы засунуть в клетку вектор, исследователю приходится прибегать ко множеству хитростей, о которых и будет сейчас рассказано. Но сначала — немного терминов.
Для внесения в клетку вектора есть несколько обозначений в зависимости от того, какой используется вектор и в какие клетки он вносится.
- Трансформация (о которой уже было немного рассказано) — это внесение плазмид (и других невирусных векторов) в бактерии, а также клетки растений и грибов;
- Трансфекция — то же самое, что и трансформация, но только в применении к клеткам животных;
- И, наконец, трансдукция — это внесение в любые клетки вирусного вектора.
Эти термины, в общем, не очень строгие. Например, даже в некоторых солидных статьях трансдукцию иногда называют вирусной трансфекцией (а то и просто трансфекцией).
Вещества-проводники
Самый простой и очевидный путь внесения в клетку генетического материала — соединить вектор с каким-нибудь переносчиком, у которого нет проблем с проникновением через мембрану, и позволить получившемуся комплексу пролезть внутрь клетки. Это не отнимает много времени и не требует дорогостоящего оборудования. Такой способ обычно называют химической трансфекцией. В этом случае события развиваются по следующему сценарию:
- Вектор соединяется с переносчиком;
- Получившийся комплекс проглатывается клеткой и оказывается в цитоплазме;
- В цитоплазме комплекс разваливается и вектор высвобождается;
- Вектор проникает в ядро и выполняет свое предназначение (скажем, с него начинает транскрибироваться мРНК).
К сожалению, почти на каждом из этих этапов возникают трудности. Во-первых, клетки захватывают далеко не все плавающие вокруг них комплексы. Во-вторых, не факт, что, оказавшись внутри клетки, вектор отделится от переносчика — вполне возможно, что они так и будут в обнимку плавать в цитоплазме, пока не подвергнутся деградации. В-третьих, даже если какой-то редкий комплекс умудрился проникнуть в клетку и там развалиться, это означает, что помимо вектора в клетке оказывается еще и переносчик, который может быть токсичен, вызывать побочные эффекты и вообще «замыливать» результаты экспериментов. И, наконец, в-четвертых, только небольшая часть вектора, оказавшегося внутри клетки, сможет проникнуть в ядро. Иными словами, комплексы вектора с переносчиком надо добавлять к клеткам в огромном избытке, чтобы хотя бы маленькая часть из них выполнила свое предназначение.
Утешает то, что среди производителей веществ-переносчиков огромная конкуренция, и поэтому на рынке постоянно появляются новые составы с улучшенными свойствами, которые минимизируют вышеописанные трудности. У каждого из составов есть какая-то своя «фишка», которая дает ему преимущество в конкурентной борьбе — некоторые образуют с вектором такие компактные комплексы, которым гораздо легче пробраться внутрь клетки; другие эффективнее отделяются от вектора, оказавшись в цитоплазме; третьи более универсальны и работают на огромном количестве типов клеток; четвертые, наоборот, славятся своей избирательностью и проникают только в те клетки, которые, например, экспрессируют какой-то специфический рецептор. Одним словом, если исследователь решил засунуть вектор внутрь клетки с помощью химической трансфекции, то ему просто надо выбрать из множества составов, представленных на рынке, тот, который будет лучше работать в данном конкретном случае.
Дырки в мембране
Но некоторые клетки так привередливы и капризны, что в принципе не соглашаются глотать комплексы ДНК с переносчиком (таким скверным характером славятся, например, первичные клетки — то есть, те, которые не выращивались в культуре, а были получены непосредственно от живого организма). Чтобы ввести в эти клетки генетический материал, ученому приходится прибегать к грубой силе — продырявливать мембрану и засовывать ДНК в образовавшиеся отверстия. Этот жестокий подход называется физической трансфекцией; он очень травматичен для клеток, и только некоторые из них переживут столь неделикатное обращение. Поэтому применять данную методику стоит, только если вы точно уверены, что обладаете достаточным количеством клеток и можете пожертвовать бóльшей частью из них. Ну и к тому же, вам потребуется довольно дорогое оборудование.
Наверное, самый распространенный способ продырявливания мембраны называется электропорацией. Дело в том, что у клеток, попавших в электрическое поле, в мембране возникают отверстия (которые получаются тем больше, чем сильнее приложенное к клеткам поле). Если эти отверстия малы, то клетка сможет «залечить» их; если же они слишком велики, то клетка погибнет из-за необратимого нарушения целостности мембраны. Поэтому эмпирическим путем можно подобрать оптимальную величину поля для того, чтобы клетки, с одной стороны, продырявились, а с другой — остались в живых. А когда клетки продырявлены, то добавленный к ним вектор проникает сквозь отверстия и оказывается в цитоплазме.
Кроме электропорации, есть еще несколько способов — экзотических и не очень — сделать в мембране дырки. Например, с помощью:
- Ультразвука (это называется сонопорация);
- Лазера (оптическая трансфекция);
- Нанопроволоки с пришитым к ней вектором, которая физически прокалывает мембрану (импалефекция);
- Магнитных взаимодействий (магнитофекция или магнитная трансфекция). В этом случае вектор присоединяется к магнитным наночастицам, которые транспортируются внутрь клетки с помощью магнитного поля.
Ну и наконец, для самых непокорных клеток, которые не поддаются никакой из вышеописанных методик, существует прибор под названием «генная пушка». Генная пушка расстреливает упрямые клетки частичками металла (обычно используется золото) с присоединенным к ним вектором. (Источником вдохновения для изобретателей этого прибора послужил пневматический молоток.) Генная пушка подходит практически для всех типов клеток, включая растительные, окруженные твердой клеточной стенкой, которая является практически непреодолимой преградой для большинства других методик.
А вообще, почти все вышеописанные методики дают более-менее похожие результаты на большей части типов клеток, а приборы для них стоят дорого. Поэтому, как правило, лаборатория покупает прибор для какой-то одной методики, и дальше уже по этой методике и доставляет генетический материал в клетки.
Овечки в волчьей шкуре
Зачем придумывать новые и трудные пути засовывания в клетку нуклеиновых кислот, если можно воспользоваться теми элегантными способами, которые за время долгой эволюции изобрели существа (или, возможно, вещества; нельзя точно сказать, живые они или нет), для которых транспортировка своего генетического материала внутрь клетки является необходимой фазой жизненного цикла? Все, наверное, уже догадались, что речь идет о вирусах.
Вирусы — это молекулы ДНК или РНК, упакованные в белковую оболочку (а иногда завернутые в липидный слой со встроенными в него вирусными белками). Именно оболочка играет главную роль в проникновении вируса через клеточную мембрану. Поэтому если засунуть в эту оболочку невирусную нуклеиновую кислоту, то она, будто вирус, тоже сможет попасть в клетку — как овечка, одетая в волчью шкуру. На этом принципе и основано использование вирусных векторов. Пожалуй, вирус — это самое эффективное транспортное средство для доставки в клетку генетического материала. Но приготовление вирусных векторов очень хлопотно, долго и трудоемко. Да вы сейчас и сами увидите.
Итак, чтобы сделать вирусный вектор, нужно для начала подобрать подходящий вирус. Идеальный кандидат:
- Стабилен — то есть, не склонен к спонтанным геномным перестройкам;
- Ёмок — то есть, может вместить в себя даже самую большую вставку;
- Не влияет на жизнедеятельность клетки;
- Не вызывает иммунного ответа;
- Встраивает свой геном не в первое попавшееся место генома хозяина (это может привести к непредсказуемым последствиям и вообще «замылить» результаты экспериментов), а в какую-нибудь определенную точку (а еще лучше — в точку, заданную самим исследователем);
- И обладает другими симпатичными чертами.
К сожалению, идеал недостижим, и ученым приходится выбирать из того, что есть. А именно:
Ретро
Ретровирусы долгое время были самой популярной основой для векторов. Это РНК-содержащие вирусы, которые, оказавшись в клетке, синтезируют ДНК на основе своей РНК с помощью ревертазы (собственно, поэтому они и называются «ретро», ведь синтез ДНК на основе РНК — это, в каком-то смысле, шаг назад). Ретровекторы хорошо выполняют свое предназначение, то есть, стабильно доставляют в клетку заключенный в них генетический материал, но у них есть несколько недостатков, из-за которых работать с ними неудобно.
Во-первых, они все (за одним исключением, о котором скоро будет рассказано) способны инфицировать только делящиеся клетки. Поэтому если исследователь, например, собрался изучать нейроны, которые не склонны к делению, ему надо забыть о ретровекторах и начать искать что-нибудь другое.
Во-вторых, ретровирусы встраиваются в самые непредсказуемые участки генома, каждый раз разные, и это приводит к самым непредсказуемым последствиям. Для начала, из-за этого нарушается воспроизводимость экспериментов — но это еще ладно. Беда в том, что ретровектор может вклиниться в середину какого-нибудь важного гена, из-за чего этот ген выключится, а в клетке начнутся патологические изменения, которые могут довести ее до гибели. Или, наоборот, ретровектор может случайно включить какой-нибудь совершенно ненужный ген, например, онкоген, что также приведет к очень печальным результатам (особенно если исследования проводятся не на культуре клеток, а на живом организме, и особенно если этот организм — человеческий).
Эти недостатки отвратили сердца ученых от ретровекторов и заставили их искать что-нибудь более подходящее. И найти кое-что замечательное удалось прямо внутри ретровирусного семейства.
Ленти
Лентивирусы — это род ретровирусов, который отличается от прочих представителей своего семейства некоторыми приятными с точки зрения молекулярного клонирования чертами.
Прежде всего, лентивирусы умеют заражать не только делящиеся, но и неделящиеся клетки. Эта особенность ужасна с точки зрения врача, который лечит вызванное лентивирусом заболевание, и прекрасна с точки зрения молекулярного биолога, который делает на основе лентивируса лентивектор. Ведь работая с таким вектором, ученый сможет использовать гораздо более широкий ассортимент клеточных типов, а значит, сделать гораздо больше великих открытий.
Плюс к тому, лентивекторы довольно емкие, то есть, они способны вместить в себя крупные вставки. Отчасти это связано с тем, что из их генома в целях безопасности выкидывается бóльшая часть, и в результате освобождается куча места. Ну и кроме того, лентивирусы встраиваются в чуть менее непредсказуемые участки генома, чем прочие ретровирусы, а это тоже очень здорово.
«Ленти» по латыни значит «медленный». Это слово очень точно отражает характер лентивирусов — они вызывают заболевания с необычайно длинным инкубационным периодом. Вирус СПИДа — это тоже, кстати, лентивирус.
Адено
Аденовирусы, наряду с ретровирусами, долго были самой популярной основой для векторов, но теперь потихоньку сдают свои позиции. Аденовирусы способны заражать не только делящиеся, но и неделящиеся клетки; ассортимент клеточных типов, которые они заражают, довольно широк. Но они не встраиваются в хозяйский геном, и поэтому подходят не для всех экспериментов. Кроме того, аденовирусы часто вызывают сильный иммунный ответ. Поэтому все чаще они используются не в базовых исследованиях, а для всяких прикладных целей — например, для создания вакцин.
И наконец, относительно недавно на сцене появился новый персонаж, который сразу расположил к себе ученых множеством чудесных качеств. Зовут его аденоассоциированный вирус (AAV).
AAV ведет себя настолько тихо, скромно и ненавязчиво, насколько этого вообще можно ждать от вируса. Практически единственное, что он делает, оказавшись в клетке, — это встраивается в хозяйский геном, причем почти всегда не в первое попавшееся, а в строго определенное место. Он, судя по имеющимся сейчас данным, не вызывает никаких заболеваний, поэтому и иммунный ответ на него очень слабый. К тому же, он способен заражать и делящиеся, и неделящиеся клетки. Одним словом, AAV — просто идеальная основа для вектора, хотя и он не лишен некоторых недостатков. И главный его недостаток — малая емкость. В AAV-вектор могут влезть только совсем небольшие вставки, и в этом он очень проигрывает, например, лентивекторам.
Кроме того, AAV — дефективный, несамостоятельный вирус. Он может размножаться только в клетках, которые уже заражены аденовирусом (что и отражено в его названии). Это совсем неплохая черта, если мы хотим заразить нашим вектором культуру клеток; но если мы собираемся делать вектор для генной терапии (методики лечения генетических (и не только) заболеваний, при которой организм заражается вирусным вектором, несущим необходимые этому организму гены), то такая дефективность будет нам очень мешать, потому что вирусы не смогут как следует распространяться по организму. Однако сейчас эта проблема решена, и разработаны AAV-векторы, которые способны размножаться сами по себе, безо всякой помощи.
Но вот подходящий вирус подобран. Теперь начинаются игры с его геномом.
- Вначале нам нужно освободить в этом геноме место — то есть, выкинуть из него какие-то гены. Обязательно нужно оставить те участки, на которые налипает оболочка (чтобы наш вектор был полноценным, «одетым» вирусом), и те гены, которые обеспечивают встраивание вирусного генома в геном хозяйской клетки (чтобы он мог выполнить свое предназначение); при этом от других областей — например, генов белков оболочки — мы можем с чистой совестью избавиться;
- Из получившегося «огрызка» генома делается плазмида — вставляются фрагменты, о которых уже было рассказано выше (точки начала репликации, селективные маркеры и так далее). В принципе, такие плазмиды уже есть в плазмидных базах данных, и, как правило, задача исследователя сводится к тому, чтобы подобрать подходящую;
- В эту плазмиду вшивается необходимая вставка (со всеми прелестями многоэтапной селекции, которые были описаны выше).
Теперь у нас возникает небольшая проблема. Даже засунув эту плазмиду в клетку, никаких вирусов мы не получим, потому что мы уже выкинули (в пункте 1) те гены, которые нужны для их создания. Поэтому нам придется пойти на маленькую хитрость.
Мы засунем в клетки не одну плазмиду, а две. Первая, основная (назовем ее Пу), — это та, которую мы получили в пункте 3. А вторая, вспомогательная (назовем ее Ме), будет нести гены, которые мы выкинули в пункте 1. Обе плазмиды начнут размножаться в хозяйской клетке. Плазмида Ме будет экспрессировать свои белки — например, белки оболочки и белки, необходимые для самосборки вирусов. Поскольку на Пу есть участки для налипания белков оболочки, то эти белки на нее и налипнут, и в результате мы получим вирус с необходимыми генами внутри, чего мы и добивались.
Итак, наш план действий таков:
- Подбираем какие-нибудь клетки, которые хорошо поддаются трансфекции (такая линия клеток называется «упаковывающей»; обычно это линия эмбриональных клеток человеческой почки НЕК293) и засовываем в них сразу две плазмиды — Пу и Ме, основную и вспомогательную;
- Ждем некоторое время (около двух дней), чтобы успели образоваться вирусы. После этого собираем среду, в которой живут клетки, — вирусы плавают в ней;
- Очищаем полученные вирусы (как правило, для этого используется центрифугирование и фильтрация) и.
- Используем их по назначению, то есть, заражаем ту линию клеток, на которой собираемся проводить эксперименты.
Это, конечно, только общая схема, у каждого конкретного вектора есть свои нюансы. Например, бывает, что вместо одной вспомогательной плазмиды используют две или даже три. При создании некоторых AAV-векторов упаковывающие клетки нужно заразить аденовирусом. А если мы создаем вектор для генной терапии, который должен уметь размножаться в хозяйской клетке и заражать ее соседей, то нам придется гораздо аккуратнее обращаться с вирусным геномом и расчищать в нем место с большой осторожностью, чтобы не нарушить способность вирусов к самостоятельному размножению. И так далее.
Последний шаг
Итак — ура! — тем или иным способом мы все-таки умудрились засунуть вектор в клетки. Нам остается последний шаг — нужно выбрать из всех клеток те, которые встроили векторную ДНК в свой геном.
Собственно, для этого мы и добавили в вектор последний селективный маркер — ген устойчивости к антибиотику, работающему на эукариотических клетках. Мы просто будем постоянно добавлять этот антибиотик в среду, в которой находятся наши клетки, — в результате останутся в живых и смогут делиться только те, которые имеют в геноме этот ген и всю нашу векторную ДНК впридачу.
Все! Клонирование завершено. Мы получили линию генетически модифицированных клеток, в геноме которых присутствует наша вставка. Пришло время проводить с этими клетками необходимые эксперименты.
Генная инженерия для биотехнологических производств
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
Генная инженерия для биотехнологических производств
1. Введение
2. Основные понятия
3. Вектор. Роль плазмидной и фаговой ДНК
4. Основные ферменты, которые использует генная инженерия
5. Этапы
5.1. Предварительный. Отбор микроорганизмов
5.2. Выделение гена. Встраивание его в вектор
5.3. Проникновение вектора
5.4. Проверка культуры на содержание вектора с геном
6. Методика слияния протопластов
7. Генная инженерия. Будущее развитие науки
8. Вывод
9. Список используемой литературы
Генная инженерия. Введение
Генная инженерия является наиболее перспективной и ведущей разработкой в сфере современных биотехнологий. Генная инженерия являет собой революционно новый способ изменения организмов путем непосредственного вмешательства в их геном. Эта наука уже находится на достаточно высоком уровне развития, однако имеет большие перспективы, предоставляя возможность решения многих проблем человечества в сфере медицины, сельского хозяйства и других областях, которые на данный момент являются довольно животрепещущими.
Сущность генной инженерии заключается в том, что, понимая признаки и свойства организма, определяемые тем или иным геном, их можно изменять, удалять или добавлять новые свойства и признаки через изменение, добавление или удаление отдельных генов.
Генная инженерия оказалась очень перспективной для медицины, прежде всего, в создании новых технологий получения физиологически активных белков, используемых в качестве лекарств (инсулин, соматостатин, интерфероны, соматотропин и другие). Инсулин используют для лечения больных диабетом, который стоит на третьем месте (после болезней сердца и рака) по частоте вызываемых смертельных случаев.
Учеными постоянно ведутся разработки препаратов для борьбы с другими сложными и неизлечимыми заболеваниям, в частности с ВИЧ-инфекцией. Сейчас ученые проводят исследования, направленные на получение особого вида белка из генно-модифицированных растений, который способен лишить вирус иммунодефицита человека вирулентности, т.е. предотвратить его распространение, а впоследствии вести профилактику СПИД.
В современной медицине для лечения различных заболеваний используется генотерапия – процесс внесения изменений в генетический аппарат клеток человека. Эта новая область в медицине в настоящее время бурно развивается и направлена на лечение заболеваний, вызванных мутациями в ДНК человека, а также придания клеткам новых функций.
Таким образом, на примере использования методов генетической инженерии в медицине, можно сказать, что генетическая модификация организмов при разумном контроле над этим процессом, способна решить некоторые серьезные проблемы современности.
Генная инженерия является одной из наиболее активно развивающихся и перспективных технологий нашего времени, которая в будущем сможет решить многие вопросы медицины и не только.
Для более четкого и детального понимания процессов генной инженерии и выполнена данная курсовая работа.
Генная инженерия. Основные понятия
Генная инженерия – это совокупность экспериментальных процедур, направленных на получение новых комбинаций генетического материала путем проводимых вне клетки манипуляций с молекулами нуклеиновых кислот и переноса созданных конструкций генов в живой организм, в результате которого достигается их включение и активность в этом организме и у его потомства.
Рекомбинантная ДНК – ДНК , полученная в результате объединения молекулы векторной ДНК , способной к репликации в определенной клетке-хозяине , с ДНК, кодирующей продукт, синтез которого желательно осуществить в этой клетке-хозяине.
Вектор – это фрагмент ДНК, обеспечивающий размножение гибридной ДНК и синтез конечных продуктов деятельности генетической системы – белков.
Ген – участок молекулы ДНК (в нек-рых случаях РНК), в к-ром закодирована информация обиосинтезе одной полипептидной цепи с определенной аминокислотной последовательностью.
Плазмида – фактор наследственности, внехромосомная кольцевая ДНК, которая обладает способностью стабильно существовать в автономном (не связанном с хромосомами) состоянии в цитоплазме.
Ген-маркер – это ген с известной локализацией и проявлением, по деятельности которого можно судить об успешности трансформации (например, гены устойчивости к антибиотикам или гены, отвечающие за синтез белков, светящихся в ультрафиолетовом свете).
Генетическая трансформация — процесс, при котором какой-либо ген (то есть уже трансген) методами генной инженерии переносится в организм. После такого переноса организм называется генетически модифицированным, или трансгенным.
Экспрессия генов — это процесс, в ходе которого наследственная информация от гена (последовательности нуклеотидов ДНК) преобразуется в функциональный продукт — РНК или белок.
Генная инженерия. Вектор
Вектор – молекула ДНК или РНК, состоящая из двух компонентов: векторной части (носителя) и клонируемого чужеродного гена. Задача вектора – донести выбранную ДНК в клетку-рецепиент, встроить ее в геном, позволить идентификацию трансформированных клеток, обеспечить стабильную экспрессию введенного гена.
Таким образом, вектор должен быть небольшим, способным поддерживаться в клетке-хозяине (реплицироваться), многократно копироваться (ампфлицироваться), экспрессировать соответствующий ген (содержать соответствующие регуляторные последовательности), должен иметь маркерный ген, позволяющий различать гибридные клетки для эффективной селекции их; должен быть способен передаваться в клетку соответствующего организма.
Существует несколько типов векторов:
Бактериальные плазмиды
Основная масса клеточной ДНК бактерий содержится в хромосоме (в хромосоме E. coli, например, 4 млн. пар нуклеотидов). Однако кроме хромосом бактерии содержат большое количество очень маленьких кольцевых молекул ДНК плазмид длиной несколько тысяч пар оснований.
Как правило, плазмиды имеют в своем составе гены устойчивости к антибиотикам, ионам тяжелых металлов (R-плазмиды), а также гены, контролирующие катаболизм некоторых органических соединений (плазмиды биодеградации, или D-плазмиды). Поскольку эти гены находятся в плазмидах, они представлены гораздо большим числом копий. Высокая копийность плазмид обеспечивает клетке синтез большого количества ферментов, химически нейтрализующих антибиотики или ксенобиотики, что и обеспечивает устойчивость к последним. Плазмиды, по-видимому, вездесущи, так как их выделяют из разных штаммов и видов бактерий, но не являются обязательными компонентами генома, а в некоторых природных штаммах плазмиды не обнаружены вообще.
Поскольку плазмидная ДНК значительно меньше хромосомной, ее довольно легко выделить в чистом виде. В присутствии ионов кальция плазмиды легко поглощаются бактериями-рецепиентами, даже если те их никогда не содержали, и в клетках бактериального потомства можно обнаружить много копий поглощенной плазмиды. Однако бактериальная клетка обычно может содержать в своем составе плазмиды одного типа. Это явление несовместимости плазмид. Существуют группы несовместимости – Inc-группы (от английского incompatibility – несовместимость). В такой группе может быть несколько плазмид, совместимых между собой, но не совместимых с другими плазмидами. У этих плазмид сходны многие признаки и часто значительна гомология ДНК.
Число копий плазмиды в клетке может существенно варьировать. Это зависит от генетических особенностей как клетки, так и плазмиды. Плазмиды, находящиеся “под ослабленным контролем”, могут размножаться до тех пор, пока их количество не достигнет 10-200 копий на клетку. Если же плазмида находится “под строгим контролем”, она реплицируется с той же скоростью, что и главная хромосома. Такие плазмиды содержатся в клетке в одной или в нескольких копиях. Естественно, что для клонирования рекомбинантных ДНК стараются использовать плазмиды первого типа. Но это не обязательно, так как плазмиды в присутствии хлорамфеникола могут умножаться независимо от деления хромосомы, и количество копий плазмиды может многократно увеличиваться.
Плазмидные векторы, как правило, создают методом генной инженерии, так как природные (не модифицированные) плазмиды лишены ряда обязательных для «высококачественного вектора» свойств:
- Небольшого размера, так как эффективность переноса экзогенной ДНК в E. Coli снижается при длине плазмиды более 15 тысяч пар нуклеотидов.
- Наличия сайта рестрикции, в который осуществлена вставка
- Наличия одного или более селективных генетических маркеров для идентификации реципиентных клеток, несущих рекомбинантную ДНК.
Если фрагмент чужеродной ДНК встраивается в один из генов устойчивости, то последний инактивируется. Следовательно, успешное встраивание фрагмента чужеродной ДНК в один из этих генов легко детектировать по исчезновению у бактерий устойчивости к данному антибиотику. Но при этом сохраняется устойчивость к другому антибиотику. Таким образом вектор дает возможность детектировать только те клоны бактерий, которые содержат рекомбинантную плазмиду.
Вирусы и бактериофаги
Есть вирусы, которые не ведут к гибели клетки, но встраиваются в геном клетки-хозяина и размножаются вместе с ней, либо вызывают ее неконтролируемый рост, т.е. превращают в раковую. К таким относятся ДНК-вирусы SV-40 и вирус полиомы. Внедрение некоторых опухолевых РНК-вирусов ведет к отпочковыванию вирусных частиц от клетки без ее лизиса. К таким вирусам относятся, например, ретровирусы (вирус саркомы Рауса и СПИДа). Для бактериальных клеток в качестве вектора часто используют бактериофаги.
Вирусы являются одними из главных кандидатов на роль векторов для введения чужеродной ДНК. При вирусной инфекции каждая клетка может получить большое число копий чужеродного гена. ДНК можно встраивать так, чтобы она находилась под контролем сильных вирусных промоторов, что обеспечит высокий уровень экспрессии гена, и его продукты будут более доступны для исследования.
Вирус должен быть жизнеспособным после рекомбинирования его ДНК. Легче всего вирусы вводятся в бактерии. Недостатком вирусов как векторов является их небольшая емкость. Кроме того, вирусы заражают небольшой круг хозяев.
Существуют гибридные вектора, содержащие ДНК фага и плазмиды.
Космиды – плазмидные вектора, в которые встроен участок генома фага λ, обеспечивающий возможность упаковки этой молекулы ДНК в фаговую частицу. Фаговые частицы обеспечивают хорошее проникновение гибридной ДНК в клетку (путем инъекции), после чего происходит замыкание ДНК в кольцо по липким концам и репликация ее по плазмидному типу.
Фазмиды также являются гибридами между фагом и плазмидой. После встройки чужеродной ДНК могут в одних условиях развиваться как фаги, в других – как плазмиды.
Вироиды
Из всех известных в настоящее время инфекционных агентов имеют ранг наиболее странных. Известно, что самые мелкие вирусы, способные к независимой репликации, имеют размеры генома, соответствующие молекулярной массе 1 М, то есть около 1500 тыс. пар оснований. Это считали минимальным количеством генетической информации, необходимой для кодирования вирусоспецифических продуктов и подавления метаболизма хозяйской клетки.
Однако в 1971 году были открыты инфекционные агенты, представляют собой очень короткую цепь 1 нитевой ковалентно связанной кольцевой РНК, состоящую из 270-300 нуклеотидов (на три порядка меньше самых минимальных вирусов), не заключенную в белковую оболочку. Это необычные патогены – самые простые и самые маленькие из всех известных.
Каким образом вироиды продуцируют симптомы болезни в инфицированных растениях, не известно до сих пор. Установлено, что они реплицируются ферментами клетки-хозяина, не транслируются в видоспецифичные полипептиды, интегрируются в геном клетки-хозяина.
Вироиды заражают персиситентно (не происходит выздоровления). Вызывают системную инфекцию, т.е. мигрируют из сайта внедрения в другие части растений, переносятся механически или через клеточный сок, через семена, пыльцу. Вироиды также связаны с ядерными фракциями растений и могут размножаться в ядрах.
При работе с вироидами получают 1-нитевую ДНК- копию РНК и достраивают комплементарную нить для получения 2-нитевой ДНК вироида. Такая 2-цепочечная ДНК вcтраивается в плазмиду и передается в клетки E. coli для клонирования. Считывание гена начинается с промотора, который узнается РНК-полимеразой, отвечающей за транскрипцию ДНК в матрицу РНК. Обычно это фрагмент ДНК из 41-44 пар оснований. Ген считывается слева направо, от 5’ к 3’ концу гена и заканчивается в терминальной области гена. За промотором начинается стартовый сайт транскрипции, за которым следует смысловая часть гена. Промоторная область гена содержит определенные короткие сочетания нуклеотидов, характерные для бактериальных генов, или для генов высших организмов. Такие сочетания служат сигналами для РНК-полимеразы, которая присоединяется к промоторной части гена и начинает его считывать.
Однонитевые и двунитевые ДНК способны инициировать репликацию вироида в механически инокулированных растениях табака. Энзиматически in vitro синтезированы также РНК вироидов, высокоинфекционные для растений. Векторные системы могут быть разработаны на основе самих РНК, на основе вироидоспецифичных ДНК, а также в комбинации вироидоспецифичных ДНК с Ti-плазмидами. Вироиды инфицируют своих хозяев в течение всего их жизненного цикла, поэтому в случае использования вироидных векторных систем можно ожидать постоянной экспрессии чужеродного гена в растении.
Хлоропластная и митохондриальная ДНК также привлекают внимание ученых в качестве возможных векторов для переноса генов в клетку. Структурная организация этих клеточных субгеномов существенно различается.
Хлоропласты и другие пластиды обладают одинаковой генетической информацией, так называемым пластомом. У высших растений он представляет собой замкнутую молекулу ДНК длиной 150 т. н. п., достаточную для кодирования примерно 100 белков. Для синтеза пластид необходимо значительно больше белков. Остальные белки кодируются ядром, синтезируются в цитоплазме и поступают в хлоропласты. Некоторые важнейшие белки хлоропластов состоят из нескольких субъединиц, часть из них синтезируется на рибосомах цитоплазмы и транспортируется в хлоропласт, где они объединяются с другими полипептидами, закодированными в самом хлоропласте и там же синтезируемыми. Таким образом, для биосинтеза функционально активного хлоропласта требуется согласованная экспрессия генома и пластома.
Гены растений также способны к экспрессии в клетках Е. coli. Это гены большой субъединцы РБФК. Преимущество хлоропластных генов заключается в том, что их экспрессия в клетках кишечной палочки может быть достигнута путем простого объединения транскрибируемых последовательностей, т.к. в ДНК хлоропластов и бактерий до начала стартовых кодонов трансляции расположена одинаковая нуклеотидная последовательность. Это дает возможность синтезировать растительные экономически важные полипептиды с помощью клеток прокариот.
В отличие от хлоропластной, ДНК митохондрий характеризуются исключительным разнообразием и их величина колеблется от 200 до 2400 т. н. п.. Однако никакой корреляции между размером митохондриального генома и числом белковых продуктов, синтезируемых изолированными митохондриями, не наблюдается. Это явление, а также большие размеры митохондриальной ДНК, по-видимому, можно объяснить присутствием ДНК, бесполезной для функционирования митохондрий.
Транспозоны
Транспозоны – сегменты ДНК, которые контролируют собственную транспозицию (перемещение) из одного сайта ДНК в другой путем вырезания из исходного сайта и внедрения в новый сайт хромосомы или плазмиды.
Механизм перемещения фрагментов ДНК по геному до конца не выяснен. ДНК переносится ферментом транспозазой. Фермент кодируется последовательность длиной около 20 нуклеотидов в середине транспозона. Он специфически взаимодействует с концевыми инвертированными повторами мобильного элемента и может вырезать его из хромосомы. Вырезание может происходить точно – с восстановлением исходной структуры участка ДНК, и неточно, то есть с делециями и вставками от одного до нескольких нуклеотидов. Это приводит к появлению стабильных мутаций и является одним из механизмов создания новых последовательностей ДНК.
Генная инженерия. Биологический смысл перемещения отдельных сегментов ДНК:
– прерывание соответствующего гена, что ведет к эволюции;
– регуляция деятельности генов, так как транспозоны могут нести сигналы для начала считывания генов. В новых областях усиливают или запрещают работу гена.
Транспозоны также участвуют в горизонтальном переносе генов.
У бактерий были обнаружены 2 класса подвижных генов, различающихся по длине и сложности организации.
1. Инсерционные последовательности, или 1S элементы, имеющие длину около тысячи пар нуклеотидов и содержащие только ген, отвечающий за их перемещение.
2. Транспозоны, длиной от 3 до 20 т. н. п., состоящие из ряда дополнительных генов, отвечающих за устойчивость бактерий к различным токсическим веществам.
Поскольку подвижные гены могут перемещаться в пределах генома с одного места на другое, то они могут быть весьма эффективными векторами для передачи рекомбинантной ДНК. Перенос генов при помощи транспозонов имеет большие преимущества, так как он происходит с высокой частотой и не влечет значительных перестроек интегрируемой ДНК. Кроме того, этим методом можно переносить достаточно большие фрагменты ДНК.
Основные ферменты, которые использует генная инженерия
Генная инженерия – потомок молекулярной генетики, но своим рождением обязана успехам генетической энзимологии и химии нуклеиновых кислот, так как инструментами молекулярного манипулирования являются ферменты. Если с клетками и клеточными органеллами мы подчас можем работать микроманипуляторами, то никакие, даже самые мелкие микрохирургические инструменты не помогут при работе с макромолекулами ДНК и РНК. Задача генного инженера – подобрать фермент, который выполнил бы поставленные задачи, то есть смог бы работать с определенным участком нуклеиновой кислоты.
Следует отметить, что ферменты, применяемые в генной инженерии, лишены видовой специфичности, поэтому экспериментатор может сочетать в единое целое фрагменты ДНК любого происхождения в избранной им последовательности. Это позволяет генной инженерии преодолевать установленные природой видовые барьеры и осуществлять межвидовое скрещивание.
Ферменты, применяемые при конструировании рекомбинантных ДНК, можно разделить на несколько групп:
– ферменты, с помощью которых получают фрагменты ДНК (рестриктазы);
– ферменты, синтезирующие ДНК на матрице ДНК (полимеразы) или РНК (обратные транскриптазы);
– ферменты, соединяющие фрагменты ДНК (лигазы);
– ферменты, позволяющие осуществить изменение структуры концов фрагментов ДНК.
Рестриктазы
Рестриктазы (рестрицирующие эндонуклеазы, эндонуклеазы рестрикции) – это ферменты, узнающие и атакующие определенные последовательности нуклеотидов в молекуле ДНК (сайты рестрикции).
Еще в 1953 году было обнаружено, что ДНК определенного штамма E. coli, введенная в клетки другого штамма (например, ДНК штамма В – в клетки штамма С) не проявляет, как правило, генетической активности, так как быстро расщепляется на мелкие фрагменты.
В 1966 году было показано, что это явление связано со специфической модификацией хозяйской ДНК – она содержит несколько метилированных оснований, отсутствующих в немодифицированной ДНК, причем метилирование (добавление к основанию метильной группы) происходит уже после завершения репликации. Бактерия способна отличить свою собственную ДНК от любой вторгающейся «чужеродной» именно по типу ее модификации. За «метку» отвечают метилирующие ферменты модификации, так называемые ДНК-метилазы. Различие в модификации делает чужеродную ДНК чувствительной к действию рестрицирующих ферментов, которые узнают отсутствие метильных групп в соответствующих сайтах.
Системы рестрикции и модификации широко распространены у бактерий; их существование играет важную роль в защите резидентной ДНК от загрязнения последовательностями чужеродного происхождения.
Поскольку разные бактерии по-разному метят свою ДНК, то и рестриктазы должны узнавать разные последовательности. И действительно, с тех пор выделены рестриктазы, узнающие более 150 сайтов рестрикции (мест расщепления ДНК).
В настоящее время известны многие десятки разных рестриктаз, дифференцируемые на рестриктазы, разрезающие либо одну из двух комплементарных нитей ДНК, либо сразу обе нити.
В результате действия рестриктаз в двухнитевой ДНК появляется щель, с двух сторон которой находится по «липкому концу». В эту щель может быть встроен ген – фрагмент ДНК, если он четко обозначен однонитевыми участками, комплементарными однонитевым липким концам, сформированным в результате действия рестриктаз на вектор. Чтобы подготовить включение гена в вектор надо использовать рестриктазу той же специфичности. Следует учесть, что липкие концы не должны образовываться в самом гене. Поэтому, имеют преимущества рестриктазы, распознающие длинные последовательности по порядку расположения пар нуклеотидов. Количество таких последовательностей в молекуле ДНК, которые обнаруживает рестриктаза, резку уменьшается по мере возрастания в них числа пар нуклеотидов. Следовательно, уменьшается возможность повредить рестриктазой сам ген, который включается в вектор в неповрежденном виде.
Все рестрикционные эндонуклеазы бактерий узнают специфические, довольно короткие последовательности ДНК и связываются с ними. Этот процесс сопровождается разрезанием молекулы ДНК либо в самом сайте узнавания, либо в каком-то другом, что определяется типом фермента. Наряду с рестрикционной активностью бактериальный штамм обладает способностью метилировать ДНК; для этого процесса характерна такая же специфичность в отношении последовательностей ДНК, как и для рестрикции. Метилаза добавляет метильные группы к адениновым или цитозиновым остаткам в том же сайте, в котором связывается рестрикционный фермент. В результате метилирования сайт становится устойчивым к рестрикции. Следовательно, метилирование защищает ДНК от разрезания.
Различают 3 основных класса рестриктаз.
Все рестриктазы узнают на двуспиральной ДНК строго определенные последовательности, но рестриктазы 1-го класса осуществляют разрывы в произвольных точках молекулы ДНК, а рестриктазы 2-го и 3-го классов узнают и расщепляют ДНК в строго определенных точках внутри сайтов узнавания или на фиксированном от них расстоянии.
Ферменты типов 1 и 3 имеют сложную субъединичную структуру и обладают двумя типами активностей – модифицирующей (метилирующей) и АТФ-зависимой эндонуклеазной.
Ферменты второго класса состоят из 2 отдельных белков: рестрицирующей эндонуклеазы и модифицирующей метилазы, поэтому в генной инженерии используются исключительно ферменты 2-го класса. Они нуждаются в ионах магния в качестве кофакторов.
Большинство рестриктаз класса 2 узнают последовательности, содержащие от 4 до 6 нуклеотидных пар, поэтому рестриктазы делят на мелко- и крупнощепящие. Мелкощепящие рестриктазы узнают тетрануклеотид и вносят в молекулы гораздо больше разрывов, чем крупнощепящие, узнающие последовательность из шести нуклеотидных пар. К мелкощепящим относятся рестриктазы Hpa II и Alu (из Arthrobacter luteus), к крупнощепящим – Eco R I (из Escherichia coli) и Hind III.
Полимеразы
Впервые ДНК-полимераза была выделена Корнбергом с сотрудниками в 1958 году из E. coli.
ДНК-полимераза I E. coli (Pol I) не связывается с молекулами двухцепочечной кольцевой ДНК. Однако, если такие молекулы денатурировать и получить одноцепочечные формы, то с последними полимераза связывается в количествах, пропорциональных длине этих участков — примерно одна молекула на 300 нуклеотидных остатков. Pol l связывается с одноцепочечными участками двойной спирали ДНК, в местах одноцепочечных разрывов с З’-гидроксилом и 5′-фосфатом, а также с концами двухцепочечных молекул ДНК.
Фермент состоит из мономерной полипептидной цепи с молекулярной массой 103 кДа и имеет 3-х доменную структуру. Каждый домен обладает своей ферментативной активностью: 5’ – 3’ полимеразной, 3’ – 5’ экзонуклезной, 5’ – 3’ экзонуклеазной.
1. 5’— 3′ полимеразная активность. Для реакции необходимо наличие одноцепочечной ДНК-матрицы и комплементарного участку этой цепи фрагмента — праймера (затравки) с З’-ОН концом.
2. 3′- 5′ экзонуклеазная активность. Гидролизует одноцепочечную или двухцепочечную ДНК с З’-ОН конца. 3’—5′ нуклеаза расщепляет диэфирную связь только в неспаренных участках ДНК. Известно, что при полимеразной реакции с определенной частотой возможно включение в растущую цепь некомплементарного нуклеотида. Однако полимераза не может присоединять нуклеотид к неправильно спаренному концу, образовавшемуся при ее участии. На помощь приходит 3’—5′ экзонуклеаза, убирающая ошибочный нуклеотид, на место которого затем присоединяется правильный нуклеотид-предшественник. 3’—5′ экзонуклеолитическая активность проявляется в направлении, обратном синтезу ДНК (см. рис. 34). Таким образом, 3’—5′ экзонуклеазная активность ДНК-полимеразы играет важную роль в точности полимеризации, направляемой матрицей.
3. 5’— 3′ экзонуклеазная активность. Деградирует одну цепь двухцепочечной ДНК, начиная со свободного 5′-конца. В отличие от 3’—5′ экзонуклеазы 5’—3′ экзонуклеаза расщепляет диэфирную связь только в спаренных участках двухцепочечной молекулы ДНК. Более того, в то время как 3’—5′ нуклеаза отщепляет одномоментно только один нуклеотид, 5’—3′ нуклеаза может вырезать с 5′- конца олигонуклеотиды длиной до десяти остатков.
Такое сочетание ферментативных активностей позволяет ДНК-полимеразе I E. coli играть активную роль в репарации повреждений ДНК in vivo.
Обратная транскриптаза
Обратная транскриптаза используется для транскрипции м-РНК в комплементарную цепь ДНК. При изучении ретровирусов, геном которых представлен молекулами одноцепочечной РНК, было обнаружено, что в процессе внутриклеточного развития ретровирус проходит стадию интеграции своего генома в виде двухцепочечной ДНК в хромосомы клетки-хозяина.
Обратная транскриптаза обладает, по крайней мере, тремя ферментативными активностями:
1) ДНК-полимеразной, использующей в качестве матрицы как РНК, так и ДНК;
2) активностью РНКазы Н, гидролизующей РНК в составе гибрида РНК – ДНК, но не одно- или двухцепочечную РНК;
3) ДНК-эндонуклеазной активностью.
Первые две активности необходимы для синтеза вирусной ДНК, а эндонуклеаза, по-видимому, важна для интеграции вирусной ДНК в геном клетки-хозяина. Очищенная обратная транскриптаза синтезирует ДНК как на РНК-, так и на ДНК-матрицах. Чтобы начать синтез, ревертазе, как и другим полимеразам, необходим короткий двухцепочечный участок (праймер).
Лигазы
ДНК-лигаза катализирует синтез фосфодиэфирной связи в 2-х цепочечной молекуле нуклеиновой кислоты. Иными словами, ДНК-лигазы сшивают рядом расположенные нуклеотиды, образуя связь между остатками сахаров. ДНК-лигазы абсолютно необходимы в процессах репарации ДНК, в процессах репликации – при удвоении цепи ДНК.
В генной инженерии используются 2 типа ДНК-лигаз, отличающихся по потребностям в кофакторах и способу действия. ДНК-лигаза E. coli в качестве кофактора использует дифосфопиридиннуклеотид, а лигаза фага Т4 – АТФ в присутствии Mg2+. Лигаза фага Т4 более универсальна, так как помимо лигирования липких концов способна катализировать реакцию воссоединения двухцепочечных фрагментов ДНК с тупыми концами. Она используется чаще.
Генная инженерия. Предварительный этап. Отбор микроорганизма
При выборе микроорганизма как потенциального продуцента учитывается ряд обстоятельств.
1. Поскольку микроорганизм будет выращиваться в производственных условиях в большом количестве и с ним будут контактировать многие работники предприятия (биологи, химики и др.), желательно, чтобы он не был патогенным. Кроме того, целевой генно-инженерный продукт, выделяемый из микроорганизма, должен иметь гарантии отсутствия даже следов микробной токсичности.
2. Проникший в клетку микроорганизма вектор с чужеродным для нее геном (или кластером генов) не должен расщепляться эндонуклеазами этой клетки, т.е генетический материал должен сохраняться. При этом рибосомы потенциального продуцента должны воспринимать информационную РНК, соответствующую чужеродному материалу.
3. Образовавшийся чужеродный для клетки белок (для биотехнолога – целевой продукт) не должен расщепляться ее протеазами, т.е. не подвергаться воздействию систем репарации клетки, гидролизующих чужеродные белки. Ослабление действия таких систем также является одним из предварительных этапов работы генного инженера с продуцентом.
4. Желательно, чтобы у потенциального продуцента чужеродного белка (целевого продукта) последний выводился из клетки в питательную среду, что значительно облегчит его последующее выделение и очистку.
Предварительная работа генного инженера начинается с самого гена, кодирующего целевой белок. К этому гену присоединяется нуклеотидная последовательность, в свою очередь кодирующая так называемую лидерную последовательность аминокислот (преимущественно гидрофобных). Синтезированный в клетке целевой продукт с такой лидерной последовательностью аминокислот с их помощью проходит через липидные слои цитоплазматической мембраны из клетки наружу. Однако в этом случае клетка продуцента должна быть изменена генным инженером. В частности, в мембране должна находиться «сигнальная протеаза», отщепляющая от генного продукта лидерную последовательность аминокислот перед его выходом в среду.
Важным предварительным этапом работы генного инженера является подбор вектора. Векторы, используемые при работе с микроорганизмами, конструируются чаще всего на основе умеренных фагов или плазмид. Преимущество плазмид перед фагами заключается в отсутствии лизиса клетки, возможного при работе с умеренными фагами.
Генная инженерия. Этап 2. Встраивание гена в вектор.
При создании нового рекомбинантного продуцента ключевым моментом в работе генного инженера является встраивание гена в вектор, точнее в ДНК векторной молекулы, например в плазмиду. Это становится возможным благодаря тому, что в распоряжении генных инженеров имеется большой набор разных по субстратной специфичности эндонуклеаз, называемых рестриктазами.
Благодаря действию рестриктаз в двухнитевой ДНК появляется щель, с двух сторон которой находится по липкому концу. В эту щель может быть встроен ген – фрагмент ДНК, если он имеет однонитевые участки, комплементарные однонитевым липким концам, сформированным в результате действия рестриктаз на вектор. Чтобы подготовить включение гена в вектор, надо использовать рестриктазу той же специфичности. Разумеется, липкие концы не должны образовываться в самом гене.
Другой прием, который может быть использован генным инженером – фланкирование гена синтетическими последовательностями нуклеотидов, т.е. получение методами биоорганической химии липких концов с заданным порядком нуклеотидов.
Ген, встроившийся в вектор, удерживается в нем вначале только за счет водородных связей между комплементарными липкими концами. Эта стадия получила название «отжиг». Для того чтобы ген оказался прочно встроенным в вектор, необходимо его закрепление ковалентными связями. Для этих целей служат ферменты – лигазы, замыкающие разрывы в углеводно-фосфатном каркасе ДНК. После этой стадии работы генного инженера вектор с прочно закрепленным в нем геном может вводится в микробную клетку.
Генная инженерия. Этап 3. Введение вектора в клетку.
Способы прямого введения генов в клетку
Прямое введение гена в клетку осуществляют несколькими способами:
- Трансфекция
- Микроинъекция
- Электропорация
- Метод «мини-клеток»
- Упаковка в липосомы
При трансфекции ДНК адсорбируется на кристаллах фосфата кальция. Образуются частицы кальциевого преципитата. Они поглощаются клеткой путем фагоцитоза.
Для повышения эффективности трансформации к специфической ДНК, содержащей ген, по которому будет производится селекция, добавляется неспецифическая ДНК-носитель. Обычно для этой цели берут ДНК из тимуса теленка или спермы лосося. Часть ДНК связывается с мембраной и не попадает в клетки. ДНК акцептируют от 15 до 90% клеток. Через несколько суток после введения небольшая доля клеток способны экспрессировать чужеродные гены, но затем уровень экспрессии падает и более или менее стабильную трансформацию претерпевает 10-3 – 10-5 клеток.
В клетки можно вводить любой ген, если заранее лигировать его с клонированным селективным маркером. Однако дальнейшие исследования показали, что лигирование вне клетки не обязательно. Клетки, поглощающие селективный ген, вместе с ним поглощают и другую ДНК, имеющуюся в кальциевом преципитате. Таким образом, пользуясь методом котрансформации, практически любой клонированный сегмент ДНК можно ввести в культивируемые клетки эукариот, если включить эту ДНК вместе с селективным маркером в состав смеси для образования кальциевого преципитата.
Для обработки клеток-рецепиентов используются грубо очищенные препараты хромосом, так как хромосомы при этом разрушаются меньше всего. Количество хромосом для обработки 1 клетки ограничено. Лучше использовать не более 20 хромосом на 1 клетку-рецепиент, так как при высоких концентрациях хромосом в суспензии они агглютинируют. Рецепиентная клетка содержит фрагменты донорных хромосом, которые могут встраиваться в геном, могут реплицироваться самостоятельно. Во введенных фрагментах часто наблюдаются делеции.
Не все клетки способны к трансформации геномной ДНК с высокой частотой. Человеческие фибробласты эффективно включают плазмидную ДНК и почти не включают геномную.
Микроинъекция ДНК в клетки млекопитающих стала возможной с появлением прибора для изготовления микропипеток диаметром 0.1-0.5 микрона и микроманипулятора. При наличии хорошего оборудования можно за 1 час инъецировать 500-1000 клеток, причем в лучших экспериментах в 50% клеток наблюдается стабильная интеграция и экспрессия инъецированных генов. Преимущество описываемого метода заключается также в том, что он позволяет вводить любую ДНК в любые клетки, и для сохранения в клетках введенного гена не требуется никакого селективного давления.
Электропорация основана на том, что импульсы высокого напряжения обратимо увеличивают проницаемость биомембран. В среду для электропорации добавляют клетки и фрагменты ДНК, которые необходимо ввести в клетки. Через среду пропускают высоковольтные импульсы (напряжение 200 – 350 В, длительность импульса 54 мс), приводящие к образованию пор (электропробой) в цитоплазматической мембране, время существования и размер которых достаточны, чтобы такие макромолекулы, как ДНК, могли из внешней среды войти в клетку в результате действия осмотических сил. При этом объем клетки увеличивается.
Напряженность электрического поля и продолжительность его действия, концентрации трансформирующей ДНК и реципиентных клеток для каждой системы клеток подбирают экспериментально, с тем чтобы достичь высокого процента поглощения ДНК выжившими клетками.
Электропорация — физический, а не биохимический метод, и это обусловливает его широкое применение.
Электропорация — наиболее простой, эффективный и воспроизводимый метод введения молекул ДНК в клетки. Однако до недавнего времени этот метод использовался в ограниченном числе лабораторий в связи с отсутствием серийных приборов — электропораторов. Появление и совершенствование таких приборов в ближайшие годы приведет к широкому применению данного подхода в генетической инженерии самых разных типов клеток.
«Мини-клетки» получают путем блокирования донорных клеток в митозе колцемидом. При продолжительной обработке клеток колцемидом в них вокруг каждой хромосомы формируется новая ядерная мембрана. Обработка цитохалазином В и центрифугирование приводит к образованию мини-клеток, представляющих микроядра, инкапсулированные в цитоплазматическую мембрану.
Полученные мини-клетки очень чувствительны к разного рода воздействиям, поэтому для слияния подбирают специальные мягкие условия. Метод трудный, капризный, эффективность низкая – 10-6 – 10-7.
Упаковка в липосомы используется для защиты экзогенного генетического материала от разрушающего действия рестриктаз.
Липосомы – сферические оболочки, состоящие из фосфолипидов. Получают их путем резкого встряхивания смеси водного раствора и липидов, либо обрабатывая ультразвуком водные эмульсии фосфолипидов. Липосомы, состоящие из фосфатидилсерина и холестерина наиболее пригодны для введения ДНК в клетки животных и растений. Системы переноса с помощью липосом низкотоксичны по отношению к клеткам.
Генная инженерия. Этап 4. Проверка культуры на содержание вектора с геном.
Ген-маркер – ген, который «легко заявляет о себе», т.е маркирует клетку и , соответственно, клон. Ген-маркер также встраивается в вектор, но с помощью другой рестриктазы. Это ген не будет иметь никакого значения в будущем биотехнологическом процессе, но он нужен для отбора продуцента целевого продукта, кодируемого рабочим геном.
Можно выделить 2 группы маркерных генов, позволяющие отличить трансформированные клетки:
1. Селективные гены, отвечающие за устойчивость к антибиотикам (канамицину, тетрациклину, неомицину и др.), гербицидам (у растений). Это могут быть гены ауксотрофности по какому-либо субстрату и т.д. Основной принцип работы такого маркера – способность трансформированных клеток расти на селективной питательной среде, с добавкой определенных веществ, ингибирующих рост и деление нетрансформированных, нормальных клеток.
2. Репортерные гены, кодирующие нейтральные для клеток белки, наличие которых в тканях может быть легко тестировано.
Чаще всего в качестве репортерных используются гены β-глюкуронидазы (GUS), зеленого флюоресцентного белка (GFP), люциферазы (LUC), хлорамфениколацетилтрансферазы (CAT). К настоящему времени из этого арсенала наиболее часто используют гены GUS и GFP и, в меньшей степени, LUC и CAT. Используемый в настоящее время как репортерный ген GUS является модифицированным геном из Escherichia coli, кодирующим β-глюкуронидазу с молекулярной массой 68 кД. GUS активен в широком диапазоне условий среды с оптимумом при рН 5-8 и 37°С.
Он может гидролизовать обширный спектр природных и синтетических глюкуронидов, что позволяет подбирать соответствующие субстраты для спектрофотометрического или флюориметрического определения активности фермента, а также для гистохимического окрашивания тканей in situ (например, в синий цвет). Фермент достаточно стабилен: он устойчив к нагреванию (время полужизни при 55°С составляет около 2 ч) и к действию детергентов. В процессе замораживания-оттаивания потери активности GUS не происходит. В составе химерных белков, созданных генно-инженерными методами, GUS обычно сохраняет свою функциональную активность. В живых клетках белок GUS также весьма стабилен и активен от нескольких часов до нескольких суток.
Генная инженерия. Методика слияния протопластов
Клеточная инженерия –«насильственный» обмен участками хромосом у прокариот или участками и даже целыми хромосомами у эукариот.
С ее помощью возможно получение межвидовых и межродовых гибридных культур микроорганизмов, а также гибридных клеток между отдаленными в эволюционном отношении многоклеточными организмами.
Для обмена фрагментами хромосом у прокариот необходимо предварительно получить из их клеток лишенные клеточной стенки протопласты; затем осуществить слияние (фузию) протопластов с образованием диплоидов; полученные диплоиды инкубировать в течение нескольких часов для ломки и воссоединения кольцевых хромосомных нитей в разных вариантах. Затем суспензию протопластов высевают на твердую питательную среду, при этом часть диплоидов превращается в гаплоиды – способные к размножению клетки, которые образуют колонии. Их изучают и отбирают культуры, приобретающие новые качества, представляющие интерес для биотехнолога.
Таким образом, первый этап работы связан с удалением у микроорганизмов клеточной стенки. У прокариот – эубактерий и актиномицетов – многоклеточных бактерий клеточная стенка состоит из жесткого полимера пептидогликана. Он может быть расщеплен с помощью ферментов (гидролаз пептидогликана), из которых самым известным является лизоцим, расщепляющий полисахаридные нити пептидогликана. Ферментативная деградация клеточной стенки в обычных условиях культивирования бактерий сразу же ведет к их лизису из-за разницы в осмотическом давлении. При этом ни цитоплазма, ни внешняя мембрана не выдерживают целостности.
Удалить клеточную стенку и сохранить целостность протопласта можно, лишь выровняв осмотическое давление внутри клетки и в среде.
Для получения протопластов клеточную стенку удаляют ферментативной обработкой в «гипертонической среде» с 20% раствором сахарозы или маннита, иногда с 10% раствором натрия хлорида в зависимости от определенных особенностей биообъекта. Превращение суспензии клеток в суспензию протопластов обычно контролируют методом фазово-контрастной микроскопии.
Следующий этап работы состоит в объединении суспензий двух образцов протопластов, принадлежащих разным штаммам или разным видам. Частота слияния резко повышается при добавлении к протопластам полиэтиленгликоля, обладающего свойствами детергента.
После промывания гипертонической средой, но уже не содержащей гидролизующего клеточную стенку ферментативного препарата, протопласты высеиваются на твердую питательную среду. При этом часть диплоидов превращается в гаплоиды – способные к размножению клетки, которые образуют колонии. Однако во время нахождения протопластов в диплоидной форме в некоторых из них происходит «ломка» и воссоединение хромосомных нитей, при котором в одну хромосому может включиться фрагмент другой. Таким образом, при регенерации протопластов формируются нормальные клетки, часть которых имеет гибридные хромосомы. Культуры таких клеток обладают новыми свойствами.
После протопластирования выявляются «плюс»- и «минус»-варианты продуцента по сравнению с производительностью исходной культуры. Отбор «плюс»-вариантов затруднений не вызывает, однако сложно добиться их длительного использования в производстве. Для замедления возвращения «плюс»-варинатов к исходным показателям предлагается два пути.
Первый – обработка мутагенами и отбор мутагенов с пониженной способностью к возвращению измененных участков ДНК к норме.
Второй связан с иммобиолизацией биообъектов. Можно связывать клетки с нерастворимыми носителями и использовать в производстве, не прибегая к пересевам в течение определенного времени.
Генная инженерия. Будущее развитие науки
Некоторые футурологи, утверждают, что человек, в принципе, может жить 1 000 лет и больше в том случае, если людям удастся разработать системы замены вышедших из строя органов. Они считают, что эта перспектива не так уж туманна, и уже сейчас есть намеки на то, что она может стать реальностью.
Например, ученые из Университета Миннесоты создали бьющееся сердце, что дает поводы надеется на то, что в будущем, вышедшие из строя органы будут с легкостью заменяться искусственно выращенными. Возможно, дальше будут не только внутренние органы.
Вообще же, считается, что у трансплантации искусственно выращенных органов есть будущее, если органы будут выращиваться из стволовых клеток того, кому требуется пересадка, потому как в этом случае новый орган не будет отторжен организмом как враждебное образование. Кроме того, есть перспективное направление в медицине – генная терапия. Например, благодаря манипуляциям с подменой и инъекцией различных генов, можно будет лечить различные заболевания.
Будущее ставит перед человечеством множество проблем, с которыми эффективно могут справляться люди высокоорганизованные, здоровые с большим интеллектуальным потенциалом. Благодаря генной инженерии и генетике можно будет выращивать отдельные положительные качества людей, как в детском, так и во взрослом возрасте. Человек будет иметь возможность усилить свои умственные способности, иммунитет и продолжительность жизни благодаря лишь внедрению определённых генов в организм. Очень заманчивая перспектива, учитывая, что многие учёные, среди которых первооткрыватели ДНК говорят о том, что глупость основывается на генетике и может быть излечима.
Генная инженерия в перспективе сможет побороть генетические заболевания, и здоровье человека поднимется на новую ступень. Люди избавятся от старения, и им не придётся наблюдать за тем, как увядают их тела. К примеру, известно, что старение вызывается сокращением теломер в процессе деления клеток. Теломеры располагаются на концах хромосом и осуществляют функцию защиты ДНК. В конце 90-х годов двадцатого столетия учёные внедрили в клетку ген, который восстанавливает белок теломеразы, отвечающий за восстановление теломер. Таким образом, учёные сделали клетку бессмертной.
С генетической инженерией связаны надежды на расширение ассортимента микробиологических удобрений и средств защиты растений, увеличение производства метана из бытовых и сельскохозяйственных отходов. Путем выведения микроорганизмов, более эффективно разлагающих различные вредные вещества в воде и почве, можно существенно повысить эффективность борьбы с загрязнением окружающей среды.
Генная инженерия имеет большие перспективы применения для совершенствования штаммов микроорганизмов сегодня кажутся почти неограниченными. Безусловно, будет развиваться такое направление, как создание штаммов-продуцентов белков человека, сельскохозяйственных животных и растений. Это направление связано не только с медициной и ветеринарией, но и с пищевой промышленностью. Близки к завершению работы по созданию микробиологической технологии производства ренина (фермента сычуга телят), используемого в сыроделии, сладкого белка — тау-матина (
в 3000 раз слаще сахара) и других продуктов. Ведутся работы по совершенствованию штаммов дрожжей, используемых в пивоварении и виноделии. Этим организмам передаются гены, которые могут обеспечить усвоение пентоз, разрушение фенольных соединений, конкурентоспособность при росте в нестерильных условиях.
Начаты работы по созданию процесса переработки крахмала в этиловый спирт с помощью бактерий, что значительно ускоряет и удешевляет его производство.
Вывод
Генная инженерия открыла принципиально новые возможности, дальнейшего развития молекулярной генетики, особенно тех ее разделов, которые связаны с выяснением особенностей устройства наследственного аппарата высших растений, животных и человека, генная инженерия позволяет менять наследственную основу любого живого организма путем непосредственного изменения генетической информации.
Благодаря генно-инженерным методам многократно повышается продуктивность традиционных микробов — продуцентов веществ, используемых в пищевой, кормовой, лекарственной, витаминной и других отраслях промышленности, становится возможным организовать микробиологическое производство принципиально новых эффективных вакцин и средств диагностики, многих ценных материалов, резко повысить эффективность использования удобрений, внести революционные изменения во многие другие сферы промышленной и сельскохозяйственной микробиологии.
Одной из главных сфер приложения генной инженерии становится селекция сельскохозяйственных растений и животных. Она дает возможность сознательно и высокоэффективно управлять наследственностью. С помощью генной инженерии появляется возможность создавать такие формы животных и растений, которые сочетают высокую продуктивность с устойчивостью к болезням, вредителям, паразитам и неблагоприятным факторам.
Вместе с тем использование методов генной инженерии требует особой осмотрительности и осторожности, поскольку затрагивает законы жизнедеятельности и эволюции. Развитию исследований в области генной инженерии в нашей стране придается большое значение.