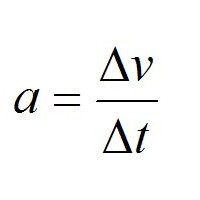В данной статье поговорим о знаке Дельта — что он из себя представляет, в каких сферах применяется и для чего вообще используется. Также вы узнаете, как выглядит знак и как его можно вставить в текст в такой программе, какой является Ворд из Майкрософт Оффис.
Знак Дельта применяется во многих сферах жизнедеятельности, к примеру, в физике, текстовых редакторах, формулах и других сферах. Чаще всего именно при печати учебной литературы, докладов и других видов документов применяют знак дельта, который имеется в разных версиях ВОРД от Виндовс и других приложениях для создания документов текстового формата на ПК.
- О происхождения знака
- Где применяется данный символ?
- Как ввести в «Ворд»?
- Система химических связей и соединений (СХСС) в виде «Химического треугольника»
- Знак дельта и его значение. Знак дельта в «Ворде»
- Откуда он пришел?
- География
- Математика
- Физика
- Астрономия и космогония
- Вводим в «Ворде»
- Любое приложение
- Альтернативный вариант – буфер обмена
- Таблица символов: оптимальное решение в любом случае
- Подведем итоги: какой способ лучше?
О происхождения знака
Появление символа связано с греческими языком, но сама буква появилась от стародревнего финийского языка, в котором именовалась – далет, что обозначало («вход в дверь»). Выглядела «далет» как перевернутый влево равнобедренный треугольник. В греческом алфавите, была такая буква. Позже эта буква дала начало всем известной буквы латинского набора – D , которая и поныне есть во многих алфавитных рядах разных государств мира, к примеру, английский алфавит ее содержит.
Буква, которая служит аналогом в русском алфавите – Д, а вот символ везде одинаков и изображается, как геометрическая фигура, а именно треугольник с равными сторонами (Δ). Эта версия является заглавной, прописная версия выглядит немного иначе, представляя собой кружок с хвостиком, похожий на обозначение в физике плотности (δ).
Где применяется данный символ?
Кроме использования в правописании греков, символ начали активно применять в математике, геометрии, алгебре, физике, химии и географии.
Поговорим отдельно о применении дельта в каждых научных сферах:
- География. Дельта подразумевает в географическом смысле начальную часть реки, океана или моря, имеет смысловое, нежели символическое, буквенное понятие и восприятие. Почему именно область впадения реки принято так называть? Все просто, дело в форме данной области, если сделать снимок сверху, то отток реки будет иметь форму правильного треугольника, а символ дельта, как раз представляет собой такой геометрический объект. Ярчайшим представителем с выраженной дельтой является река Нил (Египет), которая впадает в Средиземное море, а также Амазонка с ее впадением в океан Атлантики.
- Применение в математике, алгебре, геометрии. Очень часто знак применяют в математической сфере для таких целей, как: 1) Приращение аргумента подразумевает под дельтой измененную переменную. К примеру, сложим 5 и 4 в итоге получим число 9. Дельтой будет являться увеличение 5 на 4. 2) Применение в теории вероятности по системе Лапласа. Такой метод преподают в ВУЗах, а не школах и в нем используют такой знак. 3) А также символ применяется при обозначении прямой и обратной матриц. 4) Дельта, буква, применяемая в написании формул (как письменным методом, так и через компьютер);
- Также в математике применяют прописную версию дельта. А именно, такой символ обозначает производную от числа. Обозначение выглядит следующим образом — δy/δx. 2) Используется для описания бесконечной функции-дельта. Бесконечная функция возможна, если все значения аргумента равны нулю. 3) При помощи δ еще обозначают символику Кронекера, символ равен всегда 1, при условии того, что все его индексы равны, либо нулевые при заданных условиях.
- Физика, астрономия, космогония. Граничащие меж собой научные дисциплины, все особо важные и по-своему интересные, в каждой из дисциплин можно встретить знак дельта. В физике связь всех производных осуществляется при помощи формул с интеграцией. К примеру, формула скорости, которая выглядит следующим образом — δS к δt , является отношением одной части к другой. В данном случае расстояние, которое преодолел объект, соотносится со временем, затраченном на преодоление. Вторая производная – это ускорение, где тоже важна взаимосвязь одной составляющей формулы к другой. В космологии и астрономии применяют формулы, расчеты с данным символом, только в прописном варианте.
Как ввести в «Ворд»?
Для вставки символа заходим в верхние меню редактора и ищем колонку «Вставка», наводим на колонку курсором мыши без нажатия правой кнопки. Высвечивается несколько наименования разделов, необходимо нажать на «Символ» , где можно путем перелистывания за счет колеса мыши искать необходимый знак, либо в строке поиска выбрать категорию (статистические или математические) и найти знак. Прописной или заглавный символ высветится в рабочей области окна вставки , вам только стоит нажать правой кнопкой мыши «вставить» или «окей».
Система химических связей и соединений (СХСС) в виде «Химического треугольника»
В 2000 г. пришло понимание, что данный «Химический треугольник» несет в себе черты качественно новой — химической системы, объединяющей химические соединения (химические вещества) в единое целое [18, 41]. Ведь в отличие от Периодической системы атомов Д.И. Менделеева, объединившей атомы (физические соединения элементарных частиц), «Химический треугольник» впервые объединил базовые гомо- (простые вещества) и гете- роядерные (сложные вещества) органические и неорганические химические соединения в единое целое — химическую систему. Причем в зависимости от соотношения химических компонент связи элементов, образующих данное химическое вещество (рис. 5.2-5.5) оно имеет конкретное место в этой системе подобно атомам, находящимся в соответствующей клеточке Периодической системы атомов Д.И. Менделеева. Рассмотрим эволюцию развития и совершенствования данной системы с 1992 по 2005 гг.
Сформулируем принципиальные отличия в развитии и использовании подходов, развиваемых авторами ранее и в настоящем разделе, от отмеченных выше работ Гримма и других авторов. Они заключаются:
- 1 — в обосновании необходимости изображения перехода от одного предельного типа химической связи к другому в ряду М-К-И в виде «Химического треугольника» (XT), а не «Тетраэдра» или прямой «Линии», ввиду двух основных причин. Первая связана со спецификой химического взаимодействия (характеризуемого по Гайтлеру межъядерным обменом обобществленными электронами) в отличие от физического — ван-дер-ваальсового (в котором он отсутствует). Вторая причина связана с необходимостью учета в химической связи соединения и в тонкой структуре материалов на их основе (типа интерметаллидов) тройного метало-ковалентно- ионного смешанного типа межъядерного взаимодействия элементов;
- 2 — в комплексном обосновании возможности проведения качественной и практической реализации количественной оценки перехода различных типов связи в ряду М-К-И на основе анализа в XT изменения СОЭ и соответствующих компонент в гомо- (Ск и См) и гетероядерном (Ск , См и Си) взаимодействии элементов тонкой структуры химического соединения и материала на его основе. Определением конкретного положения связи и основных исходных классов, типов и групп металлических и неметаллических веществ на сторонах или площади XT, в отличие от ранее проведенных попыток, где это не было сделано вообще, либо проведено на интуитивном (без расчета С к , См и Си) уровне с соответствующими ошибками;
- 3 — в раскрытии методологических возможностей практического использования XT для:
- ? объединения и систематизации химических веществ и материалов на фундаментальной химической основе независимо от специфики их химической природы (металлические и неметаллические, органические и неорганические, и т.д.);
- ? прогнозирования их строения и свойств (включая агрегатное состояние) в рамках единой Системы химических связей, исходных соединений (СХСС), веществ и базовых (исходных) материалов на их основе.
В качестве фундаментальной основы, позволяющей объединить всё многообразие химических соединений в единую систему химических связей и соединений (СХСС), нами положены принципы фундаментальной индивидуальности (в смысле отличия от физических типов связи) и лабильности химической связи, которые подробно раскрыты в главе 4 настоящего учебника.
В вершинах «Химического треугольника» (рис. 5.2-5.5) авторы настоящего учебника поместили три предельных типа химических связей и соединений, а на сторонах и площади расположены примеры конкретных промежуточных типов гомо- и гетероядерных связей и соединений на их основе, иллюстрирующие закономерность перехода от предельных металлических к ковалентным и далее к ионным типам химических связей и соединений. На площади XT в качестве примера соединения с тройным типом связи приведено интерметаллическое соединение Mg3Sb2 (рис. 5.2 и 5.3). Возможность построения левой стороны «Химического треугольника» с размещением на ней в конкретных точках реальных гомоядерных химических связей и соединений была обеспечена только в результате разработанной нами в 1991-92 гг. методики количественной оценки соотношения степеней ковалентности и металличности для гомоядерных связей и соединений (см. раздел 4.3.1.2). Положение гетеросоединений на правой стороне XT вначале определялось по формуле (4.15) Л. Полинга.
Позднее было переосмыслено и уточнено качественное существо такой интегральной характеристики как СОЭ, закономерно объединяющей и одновременно разъединяющей все многообразие соединений химического уровня организации вещественной материи. Сейчас СОЭ опирается на фундаментальные взгляды классической химии и квантово-механической теории, раскрывающей специфику волновых свойств валентных (обобществленных) электронов, и рассматривает химическую связь, как универсальное явление наложения друг на друга ковалентного, металлического и ионного состояний обобществленных электронов (интеграл перекрывания). Причем две компоненты, характеризующие природу химического взаимодействия (см. выше): обменная и электростатическая (соответственно, обменный и кулоновский интегралы) определяют через СОЭ специфику равновесия локализации — делокализации обобществленной электронной плотности в межъядерном пространстве в интервале 100 >СОЭ >0 (в%). Они же обеспечивают в итоге принципиальную возможность характеристики любого промежуточного (смешанного) типа химической связи и соединения в целом.
Целесообразность графического представления этой системы, закономерно связывающей предельные и промежуточные типы химических связей и соединений (в единую систему химических связей и соединений — СХСС) в виде «Химического треугольника» (XT), а не прямой линии объясняется:
- ? существованием (в рамках существующих на сегодня моделей) трех предельных типов химических связей и соединений;
- ? необходимостью последовательного их расположения (в соответствии с изменением СОЭ) в ряду: металлические (М), ковалентные (К), ионные (И) и наоборот. Ведь еще Л. Полинг отмечал, что «можно провести систематизацию веществ по типу связи, начиная от чисто ионной через ковалентную к металлической». То есть не имеет смысла говорить о прямом или обратном металло-ионном переходе и о соответствующих химических связях и соединениях (поэтому нижняя сторона треугольника нами всегда изображалась либо вогнутой, либо пунктирной линией);
- ? необходимостью оценки смешанных связей не только с двойным типом (например, металло-ковалентным), но и более сложным тройным типом (например, ионно-ковалентно-металлическим в интерметаллическом соединении типа Mg3Sb2 (смотри рис. 5.2-5.5).
На рисунке 5.4 приведен развернутый вариант «Химического треугольника» 2002 г., который более наглядно демонстрирует черты Системы химических связей и соединений, чем варианты, представленные на рисунках 5.2 и 5.3. Появление дополнительных левых и правых сторон XT позволяет развернуть его и более полно продемонстрировать местоположение различных классов веществ и материалов.
На рис. 5.5 приведен вариант «Химического треугольника» 2005 г., который является более точным, чем вариант, представленный на рис. 5.4. Это связано с тем, что в нем впервые уточнены соотношения компонент гетеро- ядерных связей Э-О, Э-N и т.д. с определением доли металличности [42], в отличие от методики Л. Полинга, не учитывающей эту компоненту связи. В результате, положение этих гетероядерных связей и соединений в СХСС также несколько изменилось. Например, из сравнения рис. 5.4 и 5.5 следует, что для связи О-Н (в оксиде водорода, или воде) ковалентность (Ск) понизилась с 70% до 54% за счет дополнительного учета в ней металличности (См). Так же изменились и соотношения связей и в углеводородах, оксидах, карбидах и т.д. (рис. 5.4 и 5.5). Это практически очень важно, так как, например, без количественного учета металлической компоненты связи невозможно объяснить появление типичных металлических свойств (электропроводность и т.д.) у интерметаллидов и прогнозировать структуру и свойства материалов на основе бинарных и других соединений. В результате гетероядерные химические соединения и материалы на их основе должны располагаться на площади XT (см. рис. 5.5), а не на его правой стороне, как изображалось ранее (рис. 5.2 и 5.3). Поэтому в варианте 2005 г. (рис. 5.5) изображение правой стороны XT представлено пунктирной линией в силу причин, изложенных выше.
Кроме того, в варианте XT 2005 г. (рис. 5.5) вершина М (подобно вершине И) также отсутствует, так как степень металличности (См) гомосвязи (подобно Си) также не может быть равна 100%. Ведь, при См, приближающейся к или равной 100%, связь становится такой предельно делокализованной и энергетически слабой, что вещество переходит в плазмоподобное состояние, где атомные остовы вещества реально уже не связываются химическим (хотя бы частично локализованным, ковалентным) взаимодействием. Это подтверждается и тем, что наиболее химически выраженным типом связи является преимущественно ковалентная, которую открыл Льюис, назвавший ее чисто химической связью. И именно поэтому на рис. 5.4. начало химии помечено стрелкой, направленной на вершину К, соответствующую предельной 100% ковалентности гомо- и гетероядерной связи.
В области вершины К находятся минимальные по молекулярной массе биядерные соединения, типа F2 и N0, связи в которых ввиду максимальной Ск характеризуются и предельной насыщаемостью, не позволяющей им присоединить более одного элемента (КЧ = 1). А металлическая и ионная компоненты лишь в большей или меньшей степени ее «разбавляют» по мере перехода в XT от вершины К (Ск= 100%) к вершинам М и И в процессе наложения этих компонент на ковалентную компоненту.
Рис. 5.4. «Химический треугольник» единства и различия химических связей и веществ как единая система химических связей и соединений (СХСС), веществ и материалов на их основе © Сироткин О.С., 2002
Это приводит к постепенному вырождению такого свойства ковалентной связи как насыщаемость, что в начале демонстрируется ростом координационных чисел элементов молекулярных веществ, а затем при переходе границы 50/50% (рис. 5.2-5.5) и окончательной утрате этого свойства у металлических и ионных соединений. Поэтому Ск не может быть равна 0, так как это означает фактическую ликвидацию химического взаимодействия между атомными остовами и превращение химической связи в чисто физическую связь, в которой нет места обменному взаимодействию между ядрами и обобществленными электронами, а степень обобществления электронов (СОЭ) становится равной 0%.
Влияние химической связи (через соотношение двух или трех ее компонент) на местоположение исходных, или начальных, базовых, классов (IJI), типов (молекулярных — дискретных и немолекулярных — непрерывных), и групп химических соединений (ХС) в единой системе (СХСС) в виде «Химического треугольника», а также основные уровни их периодичности приведены на рис. 5.4 и 5.5. В результате, в вершине К «Химического треугольника» (рис. 5.4 и 5.5) располагаются ковалентные химические соединения, характеризующиеся предельным (100%) значением ковалентности (К), а ближе к вершинам М и И химические связи и соединения с максимальной, но не предельной (100%) металличностью (М) и ионностью (И), которые закономерно различаются значениями СОЭ (соответственно 100, 50 и 0%, которые указаны на рис 5.3 и 5.4). В скобках на левой и правой сторонах XT и дополнительных осях указаны степени ковалентности соответствующих гомо- и гетеросвязей.
Таким образом, на левой стороне XT лежат гомоядерные смешанные ковалентно-металлические (КМ) и металло-ковалентные (МК) химические связи и соединения, а на площади XT располагаются смешанные типы химических связей и соединений с тройным типом химического взаимодействия — ИКМ, КИМ, МИК, ИМК, МКИ и КМИ. Данная аббревиатура предполагает наличие двух (К и М) или трех (К, М и И) компонент в гомо- и гетероядерных связях, а последовательность их расположения определяется возрастанием вклада каждой из компонент.
Например, аббревиатура МК свидетельствует о том, что мы имеем дело с гомоядерной связью и соединением, в которых ковалентная компонента связи преобладает над металлической, обеспечивая способность данного вещества к образованию молекул, т.е. химических соединений дискретного (ХСД) молекулярного типа (СЬ и т.д.) или полимерного тела (алмаз и т.д.) постоянного состава (дальтонид) ). Аббревиатура КМ свидетельствует, что в данном гомосоединении металличность связи преобладает над ее ковалентностью и мы имеем дело с химическим соединением непрерывного (ХСН) немолекулярного типа (бертоллид) металлической группы химических соединений на основе (Э’)м.
Рис. 5.5. «Химический треугольник» как единая система химических связей и соединений (СХСС), веществ, металлических и неметаллических материалов на их основе © Сироткин О.С., 2005
Таким образом, в рамках СХСС (рис. 5.5) на основе единых химических характеристик впервые стало возможным создание универсальной классификации химических соединений с разделением их на разных уровнях:
- ? гомо- и гетероядерные классы (I, II);
- ? химические соединения дискретного (ХСД) — молекулярного типа (дальтониды) и надмолекулярные ассоциаты и агрегаты на их основе (ХХСД, где ХСД > 2); в том числе, ковалентные группы химических соединений, в виде Э’г и Э’Э» — гомо- и гетероядерных низко- или мономолекулярных (1а, Па и На’), а также [Э 1 — Э’]п и [Э’ — Э»]п — гомо- и гетероядерных олиго-, высоко (макро) молекулярных (lb, НЬ и ПЬ’) на основе ковалентных связей;
- ? химические соединения непрерывного (ХСН) — немолекулярного типа (бертоллиды) , в том числе, металлические группы химических соединений на основе (Э’)м — гомоядерных (1с — чистые металлы) и (Э’Э»)м — гетероядерных (Нс’ — сплавы) металлических связей, а также, ионные группы химических соединений, на основе (Э’Э»)и гетероядерных ионных связей (Пс).
- ? различные варианты молекулярных (ХСД) и немолекулярных (ХСН) химических соединений с тройным промежуточным (ИМК) типом связи. Например, гетероядерная связь Mg — Sb в интерметаллиде Mg3Sb2 (На’, ПЬ’ и Пс’). Строго говоря, вероятность нахождения химических связей и соединений в области (На, Пв и Нс) на правой стороне XT минимальна, так как это возможно лишь в случае полного отсутствия в гетероядерной связи металлической компоненты. Однако существование ИК или КИ связей более реально, в отличие от связей МИ или ИМ смешанного типа, так как в соответствии с единой моделью химической связи (глава 4) последних (нижняя сторона XT на рис. 5.2-5.5 отсутствует) не может быть в принципе. Но и число связей и соединений, находящихся непосредственно на правой стороне XT, также стремится к нулю или фактически минимально.
Знак дельта и его значение. Знак дельта в «Ворде»
Достаточно часто приходится в процессе набора различных документов вводить нам знак дельта. Именно его значение, а также способы ввода в различных приложениях под управлением такой ОС, как «Виндовс», и будут рассмотрены в этой статье.
Откуда он пришел?
Сам знак дельта пришел к нам из греческого языка. Это одна из букв его алфавита. На сегодняшний день ученые считают, что она послужила прародителем латинской буквы D, которая присутствует в большинстве алфавитов стран Европы и не только. В нашем же языке ее аналогом является «Д». Большой символ данной буквы – это равнобедренный треугольник, у которого в основании расположена самая маленькая сторона (то есть «Δ»). В свою очередь, прописной буквой является маленький круг с характерным верхним хвостиком (он выглядит так: «δ»). Чуть позже эти символы начали активно использоваться в различных сферах человеческой жизни, среди которых можно выделить математику и географию.
География
Широко используется данное понятие в географии. Здесь под этим термином скрывается область впадения реки в море или океан. Сверху она выглядит как треугольник. То есть аналогия здесь налицо, и подобное определение в этом случае более чем оправданно. Наиболее яркие примеры – это реки Нил (впадает в Средиземное море в северной части Африканского континента) или Амазонка (впадает в Атлантический океан и расположена в Южной Америке). С высоты птичьего полета места на стыке суши и воды этих двух великих рек действительно выглядят, как греческая буква Δ.
Математика
Значительно чаще и больше используется знак дельта в математике. Здесь он может обозначать следующее:
- Приращение аргументов. То есть за этим понятием скрывается величина, на которую изменилась переменная. Например, 2+3=5. В этом случае 2 увеличилась на 3. Это и есть Δ.
- Еще один случай, при котором используется эта буква греческого алфавита, – оператор Лапласа.
- Последний вариант, при котором используется Δ, — это обозначение определителя матрицы.
Это все справедливо для заглавной буквы. А вот с прописным символом ситуация аналогичная. Он может обозначать такое:
- В обозначении производной: δy/δx (аналогичным образом производная выглядит в физике, астрономии и космогонии).
- При описании дельта-функции, которая может быть равна бесконечности при аргументе ноль и нулю при всех остальных его значениях.
- С ее помощью обозначается символ Кронекера — δij. Он равен единице при равенстве индексов и нулю во всех остальных случаях.
В общем, не так уж и редко в современной математике можно встретить этот символ.
Физика
Еще одна сфера, где эта греческая буква повсеместно используется, — это физика. Большая часть величин этой науки связаны между собой в виде интегралов и производных. Например, скорость — это отношение δS к δt, то есть пройденного расстояния ко времени, за которое оно преодолено. В свою очередь, производной второго порядка от скорости по времени будет ускорение. Это лишь один из примеров, который показывает то, насколько важна эта греческая буква для современной физики.
Астрономия и космогония
Не меньшее значение греческая δ имеет и для этих наук. Здесь опять-таки многие величины взаимосвязаны между собой с помощью интегралов и производных. Именно последнее понятие и обозначается прописной буквой дельта.
Вводим в «Ворде»
Наиболее просто вставить в текст документа знак дельта в «Ворде» — с него и начнем. В первом случае в открытом окне данного приложения необходимо перейти на вкладку «Вставка» главного меню. Затем находим пункт с надписью «Символы». В нем открываем выпадающий список «Символ» (рядом с ним нарисована буква «омега», она по виду напоминает подкову). В нем выбираем пункт «Другие символы» (расположен в самой нижней части этого списка). Затем путем перемещения по таблице всех доступных для ввода знаков находим нужный из них и вставляем в рабочую область приложения. Затем закрываем ранее открытое окно.
Второй вариант в текстовом процессоре «Ворд» основан на использовании редактора формул. Порядок набора в этом случае идентичный. Разница состоит лишь в том, что в пункте «Символы» выбираем не выпадающий список «Символ», а перечень «Формула». Затем выбираем пункт «Новая формула». Потом на месте главного меню появится панель «Конструктор». В ее разделе находим подраздел «Символы». Затем, перемещаясь по нему, находим Δ (для заглавной буквы) или δ (в случае прописной). Потом с помощью клавиши «Таб» или указателя мыши нажимаем кнопку с надписью «Вставить». Далее закрываем окно вставки. В рабочей области текстового процессора должен появиться нужный нам символ.
Любое приложение
Можно набрать знак дельта на клавиатуре. Для этого нужно использовать АСКИ – код данного символа, который равен 916. Этот способ универсален и работает во всех приложениях под управлением ОС «Виндовс». Порядок набора в этом случае следующий:
- Переключаем язык ввода на английский.
- Переводим расширенную клавиатуру из режима навигации в режим ввода чисел. Для этого нажимаем клавишу «Нам Лук» до тех пор, пока ее светодиод не загорится.
- Переводим курсор в ту область приложения, в которой нужно набрать Δ с применением манипулятора.
- Зажимаем «Alt» в левой части клавиатуры.
- На следующем этапе необходимо ввести последовательно набор чисел, соответствующий символу дельта. Код знака у него — 916, как было отмечено ранее. Поэтому и набираем сразу 9, затем 1 и в конце 6.
- Отпускаем ранее зажатую клавишу «Alt». После этого в рабочей области нашего приложения должен появиться необходимый нам символ.
Кстати, можно код знака дельта в «Ворде» выяснить, если вы не знаете или забыли. Для этого достаточно по ранее приведенной методике зайти в окно вставки символа, найти в нем Δ, выделить его. В нижней части в поле «Код знака» и будет указана интересующая нас информация. Причем так можно узнать этот параметр для любого символа. Этот же метод ввода можно использовать и при наборе прописной буквы. Единственное отличие – это то, что у нее код 948. То есть вместо 916 нужно этот порядок чисел применить. Минус данного способа состоит в том, что необходимо помнить АСКИ-коды. Если цифр в нем от одного до трех, то еще можно запомнить. А при большем количестве символов этот метод уже не эффективно использовать.
Альтернативный вариант – буфер обмена
Еще один способ – это использовать буфер обмена, для того чтобы вставить «дельта». Знак треугольник нужно найти в любом приложении (например, на любом интернет–ресурсе). Выделить его с помощью манипулятора. Затем используется комбинация клавиш «Ctrl» и «Insert» (выполняем операцию копирования). Переходим в то приложение, в котором нужно этот символ вставить (можно использовать комбинацию «Alt» и «Tab» или указатель мышки). Затем нажимаем «Shift» и «Insert» (выполняем операцию вставки). После этого справа от курсора должен появиться символ Δ. Аналогичным образом можно вставить и прописную букву. Минус этого способа состоит в том, что нужен исходный знак. А не всегда есть возможность его найти. Поэтому это можно сделать только на компьютерах, которые подключены к глобальной паутине. В ней легко и просто можно найти исходный символ. В остальных случаях этот способ не рационально использовать.
Таблица символов: оптимальное решение в любом случае
Не всегда инсталлирован на компьютере текстовый процессор «Ворд». ЭВМ может быть не подключена к глобальной паутине и копировать знак дельта просто неоткуда. А АСКИ-код этого символа не помним. Как бы получается безвыходная ситуация. Но решение есть. Причем очень простое. Достаточно использовать такую стандартную утилиту, как «Таблица символов». Для этого выполняем следующие манипуляции:
- Открываем меню «Пуск» с помощью нажатия соответствующей клавиши или кликом правой кнопки манипулятора типа мышь.
- В открывшемся списке необходимо выбрать пункт «Программы».
- На следующем этапе кликаем на надписи «Стандартные».
- Далее нужен раздел «Системные».
- Тут находим утилиту с надписью «Таблица символов».
- В списке находим нужную нам букву (заглавную Δ или прописную δ).
- Затем совершаем клик правой кнопкой мышки на кнопке «Выбрать». После этого должна активной стать другая кнопка – «Копировать». Ее и нажимаем. Затем выбранный нами символ помещается в буфер обмена.
- Далее переходим в то приложение, в котором необходимо вставить такой символ и нажимаем стандартную комбинацию «Ctrl» и «V». В качестве альтернативы можно использовать «Shift» и «Insert». Еще один способ вставки – это использование меню «Вставка» и одноименной кнопки.
В отличие от всех ранее приведенных методов, этот является универсальным и работает во всех программах под управлением такой операционной системы, как «Виндовс».
Подведем итоги: какой способ лучше?
Очень часто в процессе набора формул в математике, физике, астрономии и космогонии используется знак дельта, как заглавный, так и прописной. Поэтому важно его вводить именно в электронном виде документа. Проще всего вставить знак дельта в «Ворде» с помощью закладки «Вставка» и подпанельки «Вставка символа». Но это частный случай, и работает он только в этом текстовом процессоре. В остальных случаях наиболее рационально использовать «Таблицу символов». При этом нет необходимости помнить специальные трехзначные АСКИ-коды или искать исходную букву, как в случае с буфером обмена. Тем более что эта утилита автоматически инсталлируется на все ПК в процессе установки операционной системы «Виндовс».